低分子化合物を収着しづらい肝臓チップで代謝試験、毒性試験が可能に:医療技術ニュース
京都大学 iPS細胞研究所CiRAは、低分子化合物を収着しづらいフッ素系エラストマー製のマイクロ流体デバイスを用いて肝臓チップを作製し、薬物収着の影響を最小限にした薬物代謝、毒性試験が可能であることを示した。
京都大学 iPS細胞研究所CiRA(サイラ)は2021年9月16日、低分子化合物を収着しづらいフッ素系エラストマー製のマイクロ流体デバイスを用いて、肝臓チップを作製したと発表した。同チップを用いて、薬物収着の影響を最小限にした薬物代謝、毒性試験が可能であることを確認した。
創薬研究におけるin vitro試験では、マイクロ流体デバイス上で細胞を培養して作製するOrgans-on-a-chip(臓器チップ)の活用が期待されている。マイクロ流体デバイスの素材としては、ポリジメチルシロキサン(PDMS)エラストマーが一般的だが、低分子化合物を収着しやすく、創薬領域では限定的な利用にとどまっていた。
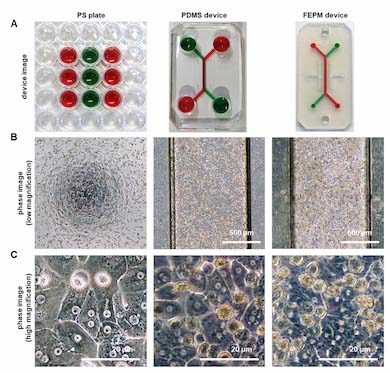
今回の研究では、低分子化合物をほぼ収着しないテトラフルオロエチレン-プロピレン(FEPM)エラストマーを素材として作製したマイクロ流体デバイスと、PDMS製マイクロ流体デバイス、細胞培養に広く用いられているポリスチレン製マルチウェルプレート(PSプレート)の3種類について性能を比較した。
まず、各デバイス上でヒト肝細胞を培養したところ、いずれもヒト肝細胞の典型的な特徴が確認できた。しかしFEPM製デバイスとPDMS製デバイスは、PSプレートと比べると細胞の形態観察がやや難しいことが明らかとなった。
次に、FEPM製デバイスでの培養がヒト肝細胞の肝機能に与える影響を調べるため、肝細胞マーカーの遺伝子発現とタンパク質発現を解析した。その結果、FEPM製デバイスで培養したヒト肝細胞は、PDMS製デバイスやPSプレートで培養した細胞と同等の機能を持つことが分かった。
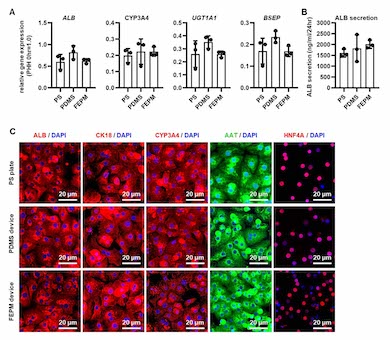 各デバイスで培養したヒト肝細胞における解析結果。A:肝細胞マーカーの遺伝子発現。B:培養上清中のヒトALB分泌量をELISAで測定した結果。C:ALBやCYP3A4など肝細胞マーカーの免疫染色結果。DAPI(青)で核染色している[クリックで拡大] 出所:京都大学 iPS細胞研究所CiRA
各デバイスで培養したヒト肝細胞における解析結果。A:肝細胞マーカーの遺伝子発現。B:培養上清中のヒトALB分泌量をELISAで測定した結果。C:ALBやCYP3A4など肝細胞マーカーの免疫染色結果。DAPI(青)で核染色している[クリックで拡大] 出所:京都大学 iPS細胞研究所CiRA続いて、FEPM製肝臓チップが医薬品の毒性試験や代謝試験に利用できるかを検討した。肝細胞毒性を誘発するクマリンを用いた毒性評価試験では、FEPM製デバイスとPSプレートのヒト肝細胞の生存率は同等だったが、PDMS製デバイスでは高く、肝細胞毒性が生じにくいことが示された。
また、薬物を添加した培地で細胞培養した後に培地中の薬物と代謝物の濃度を測定する薬物代謝試験では、FEPM製肝臓チップがPDMS製肝臓チップよりも低分子化合物の代謝物をより高感度に検出できることを確認した。
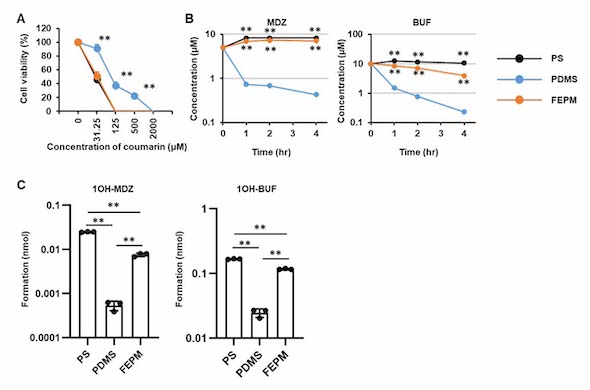 各デバイスで培養したヒト肝細胞に対し、A:クマリンを作用させ細胞生存率を測定した。B:薬物(MDZ、BUF)を含む培地で培養後、培地中のMDZやBUFなどの濃度を測定した。C:各代謝物(1OH-MDZ、1OH-BUF)の濃度を測定した[クリックで拡大] 出所:京都大学 iPS細胞研究所CiRA
各デバイスで培養したヒト肝細胞に対し、A:クマリンを作用させ細胞生存率を測定した。B:薬物(MDZ、BUF)を含む培地で培養後、培地中のMDZやBUFなどの濃度を測定した。C:各代謝物(1OH-MDZ、1OH-BUF)の濃度を測定した[クリックで拡大] 出所:京都大学 iPS細胞研究所CiRA研究チームは、2019年にFEPM製デバイスを開発していたが、細胞を搭載したFEPM製臓器チップで低分子化合物による細胞応答を評価できるかは検討していなかった。今回の研究で、PSプレートやPDMS製デバイスと、FEPM製デバイスで培養したヒト肝細胞の肝機能が同等であること、クマリンやMDZ、BUFなどPDMS製デバイスに吸収されやすい物質についても毒性検出や代謝試験が可能であることが確認された。今後の創薬研究におけるFEPM製デバイスの活用が期待される。
- 知人より見知らぬ他人とシンクロ? スポーツ観戦の熱狂を科学的に解明
- 厚さ約25μmの神経シートを開発、光刺激と記録を同時に実現
- 生きた乳酸菌は代謝、死んだ乳酸菌は免疫へ 状態で異なる腸内効果
- あなたの「網膜」は実年齢より老けている? 写真1枚でAIが疾患リスクを推定
- 50万人の情報が流出した英国バイオバンクのインシデントでPETs利用は拡大するか
- ミカンの1種“タチバナ”にシミ抑制効果、メラニンの蓄積を阻害
- セラミド不足がアトピー性皮膚炎の直接原因であることを実証
- エッジAI搭載の前眼部検査機で白内障など早期発見へ、従来機より低コスト化も
- 外科医と対話する生成AI、胃がん手術の実証実験で有用性80%達成
- 医療機器大手ストライカーの事例に見る米国サイバーインシデント情報開示の複雑性
関連記事
 小さな切開で細胞シートを心臓に移植できるデバイスを開発
小さな切開で細胞シートを心臓に移植できるデバイスを開発
京都大学は、iPS細胞などから作られた細胞シートを、手術負担の少ない内視鏡を用いて心臓表面に移植するためのデバイスを開発した。成人男性の3Dプリントシミュレーターを用いて、確実かつ歪みなく、細胞シートを移植する手技を確立した。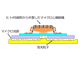 人工心臓の機能を評価する、iPS細胞由来のオーガンオンチップを開発
人工心臓の機能を評価する、iPS細胞由来のオーガンオンチップを開発
理化学研究所は、ヒトiPS細胞技術と微細加工によるマイクロデバイス技術を用いた「ハートオンチップ型マイクロデバイス」を開発し、高感度な人工心臓の機能評価系を確立した。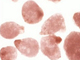 細胞の3次元培養法の自動化技術を開発
細胞の3次元培養法の自動化技術を開発
日立製作所は、同社のiPS細胞大量自動培養装置を用いて、細胞の3次元培養法の新たな自動化技術を開発した。また、細胞の自動製造プロセス構築支援サービスの提供も開始した。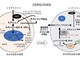 iPS細胞とES細胞の分化状態が培養液の解析のみで判断可能に
iPS細胞とES細胞の分化状態が培養液の解析のみで判断可能に
島津製作所、神戸医療産業都市推進機構、東京エレクトロンは、細胞を壊さずに細胞の分化状態を判断できる手法を見出した。細胞の品質をリアルタイムかつ非侵襲的に、容易に管理できることから、安全で有効な細胞治療につながることが期待される。 ヒトiPS細胞由来の網膜色素上皮細胞シートの自動培養に成功
ヒトiPS細胞由来の網膜色素上皮細胞シートの自動培養に成功
日立製作所と理化学研究所は、ヒトiPS細胞由来の網膜色素上皮のシート状組織「RPE細胞シート」を自動培養することに成功した。再生医療用細胞の品質が均一化し、量産による細胞の安定供給が可能になるため、再生医療の普及に貢献する。 再生医療に活用できるiPS細胞大量自動培養装置を製品化
再生医療に活用できるiPS細胞大量自動培養装置を製品化
日立製作所は、iPS細胞大量自動培養装置「iACE2」を製品化した。完全閉鎖系の流路モジュールを用いて、再生医療に使用するiPS細胞を無菌環境で播種(はしゅ)、培養、観察でき、品質の高い細胞を安定的に供給する。
関連リンク
Copyright © ITmedia, Inc. All Rights Reserved.
医療機器の記事ランキング
- 脳動脈瘤の治療をより安全に テルモが細径対応の新デバイス発売
- 厚さ約25μmの神経シートを開発、光刺激と記録を同時に実現
- 約10秒で検温完了 ケースごと丸洗い可能なテルモの新型体温計
- 知人より見知らぬ他人とシンクロ? スポーツ観戦の熱狂を科学的に解明
- 生きた乳酸菌は代謝、死んだ乳酸菌は免疫へ 状態で異なる腸内効果
- 日立ら肺がん細胞診の新解析技術 SEMと元素分析で検体評価を支援
- 75秒で精子濃度など20項目を自動解析 男性不妊検査向け装置を提案
- 50万人の情報が流出した英国バイオバンクのインシデントでPETs利用は拡大するか
- あなたの「網膜」は実年齢より老けている? 写真1枚でAIが疾患リスクを推定
- がんの微小病変解析をより正確に、1台で核酸抽出から定量を自動処理する装置
コーナーリンク