血液から直接神経細胞を生み出す技術を開発:医療技術ニュース
慶應義塾大学と藤田医科大学は、末梢血細胞からiPS細胞への初期化を介さずに神経細胞を産生する技術を開発した。誘導前の細胞が保有していた情報の一部を受け継ぐ神経細胞が、遺伝子導入から約20日で産生する。
慶應義塾大学は2025年5月26日、完全に初期化させない部分的リプログラミングという方法を応用し、末梢血細胞からiPS細胞への初期化を介さずに神経細胞を産生することに成功したと発表した。藤田医科大学との共同研究による成果だ。
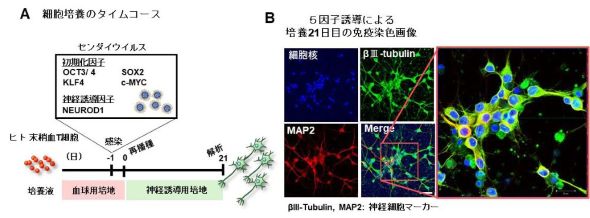
新たに開発した神経細胞誘導技術は、神経細胞の誘導に重要な転写因子NEUROD1と、iPS細胞の樹立で用いられるOCT3/4、SOX2、KLF4、c-MYCの4遺伝子を同時に末梢血T細胞に導入することで、多能性幹細胞の状態へ完全に初期化することなく神経細胞に転換させる方法だ。この方法では、遺伝子導入から約20日で神経細胞が出現する。
細胞死による減少を最小限にすべく工夫した結果、最初に利用した血液細胞数とほぼ同数の神経細胞を得られるようになった。また、同培養法の改良を重ねることで、NEUROD1遺伝子と初期化4遺伝子の5遺伝子だけで神経細胞が産生できることが分かった。
産生した神経細胞を電気生理学試験や遺伝子発現解析で調べたところ、主にグルタミン酸作動性神経細胞であることが判明した。さらに、1細胞RNAシーケンスやCre-LoxP技術による細胞系譜試験の結果から、産生した神経細胞の多くがほぼ直接的に血液細胞から神経細胞や神経幹細胞に転換されたものであることが示された。
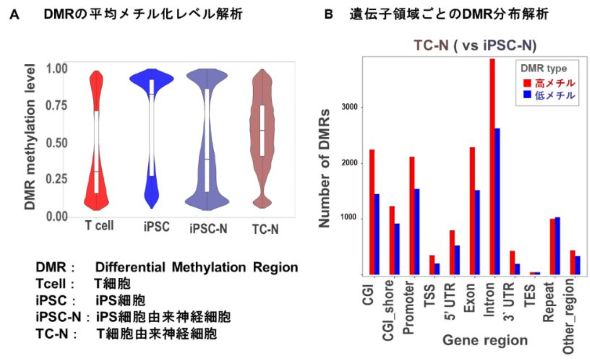
また、全ゲノムバイサルファイトシーケンスの結果から、産生した神経細胞は、誘導前の末梢血T細胞が保有していたエピジェネティックメモリー(後天的に取得した細胞情報)の一部を受け継いでいる可能性が示された。
iPS細胞の利活用は、脳神経系疾患の研究において有効な手段の1つになっている。しかし、iPS細胞を利用する手法は、例えばヒトの神経細胞を新しく調製する場合、約半年の期間を要するなど、長い時間を要する。また、細胞が初期化されることでエピジェネティックメモリーのほとんどが消失し、病態情報が保持されない懸念もある。これらの問題点を解決する方法として、直接的な神経細胞誘導法があるが、主に皮膚線維芽細胞を使用することから、細胞採取のために皮膚の切開と縫合が必要で患者への侵襲性が高かった。
今回開発した手法は末梢血を使用するため、迅速かつ簡便に多くの神経疾患患者の血液から神経細胞を作り出すことが可能になる。また、後天的に細胞が得たエピジェネティック状態に関与する病態も解析できる可能性がある。今後、創薬や再生医療への応用が期待される。
関連記事
 手のひらサイズの血管チップでがん転移過程の一部を可視化
手のひらサイズの血管チップでがん転移過程の一部を可視化
東京大学は、3次元の血管構造周囲にがん細胞集団を配置した3次元in vitroモデル「がん-微小血管チップ」を開発し、がん細胞が血管に浸潤しがん細胞の塊を形成するまでの一連のプロセスを可視化した。 日本市場で本格展開 フローズンが歯科用3Dプリンティング製品群を一挙投入
日本市場で本格展開 フローズンが歯科用3Dプリンティング製品群を一挙投入
フローズンジャパンは、デジタルデンティストリーに対応した、次世代の歯科用3Dプリンティング製品群を日本市場で本格展開する。第1弾として、歯科用3Dプリンタと歯科用2次硬化機、歯科用洗浄機、樹脂混合ステーションを販売する。 空気清浄機とフィルター付き空調により室内の飛沫濃度を大幅に削減
空気清浄機とフィルター付き空調により室内の飛沫濃度を大幅に削減
産業技術総合研究所とダイキン工業は、空気清浄機や空気調和設備の配置が室内の粒子濃度に与える影響を評価し、適切な配置によって室内の粒子量を最大88%削減できることを確認した。 ウェアラブルサーモデバイスシリーズのハイエンドモデルを発売
ウェアラブルサーモデバイスシリーズのハイエンドモデルを発売
ソニーサーモテクノロジーは、首元に装着して、本体接触部分の体表面を冷やしたり温めたりする「REON POCKET」シリーズのハイエンドモデル「REON POCKET PRO」を発売した。 エプソンが協働ロボット開発、ラボ使用も想定しクリーンルーム対応/Pythonも
エプソンが協働ロボット開発、ラボ使用も想定しクリーンルーム対応/Pythonも
セイコーエプソンが協働ロボットを開発した。2025年内をめどに日本および欧州で発売する。 VRで自分が飛べるという体験をすると高所恐怖が低減することが明らかに
VRで自分が飛べるという体験をすると高所恐怖が低減することが明らかに
情報通信研究機構は、VRで自分が飛べるという体験をすることで、高所恐怖反応が低減することを発見した。恐怖の低減度は、飛行体験によって「自分は飛行できるので落下しても危険ではない」と感じた程度と相関する。
関連リンク
Copyright © ITmedia, Inc. All Rights Reserved.
医療機器の記事ランキング
- 脳動脈瘤の治療をより安全に テルモが細径対応の新デバイス発売
- 約10秒で検温完了 ケースごと丸洗い可能なテルモの新型体温計
- 厚さ約25μmの神経シートを開発、光刺激と記録を同時に実現
- 知人より見知らぬ他人とシンクロ? スポーツ観戦の熱狂を科学的に解明
- 生きた乳酸菌は代謝、死んだ乳酸菌は免疫へ 状態で異なる腸内効果
- 日立ら肺がん細胞診の新解析技術 SEMと元素分析で検体評価を支援
- あなたの「網膜」は実年齢より老けている? 写真1枚でAIが疾患リスクを推定
- 50万人の情報が流出した英国バイオバンクのインシデントでPETs利用は拡大するか
- がんの微小病変解析をより正確に、1台で核酸抽出から定量を自動処理する装置
- 猛暑の夏を乗り切る! 冷却性能20%増の首元デバイスで−2℃体験へ
コーナーリンク
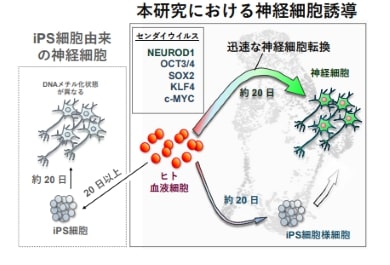 研究の概要 出所:慶應義塾大学
研究の概要 出所:慶應義塾大学