人工心臓の機能を評価する、iPS細胞由来のオーガンオンチップを開発:医療機器ニュース
理化学研究所は、ヒトiPS細胞技術と微細加工によるマイクロデバイス技術を用いた「ハートオンチップ型マイクロデバイス」を開発し、高感度な人工心臓の機能評価系を確立した。
理化学研究所は2020年11月5日、ヒトiPS細胞技術と微細加工によるマイクロデバイス技術を用いて「ハートオンチップ型マイクロデバイス」を開発し、高感度な人工心臓の機能評価系を確立したと発表した。
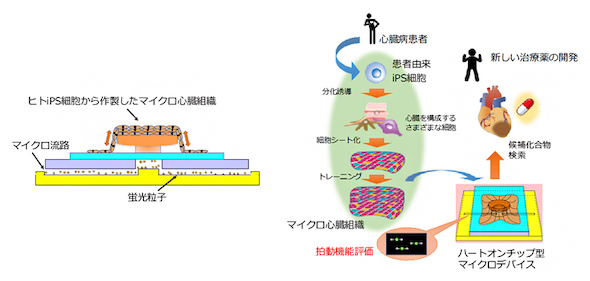
ハートオンチップ型マイクロデバイスは、オーガンオンチップ(Organ-on-a-chip)の1種で、マイクロ心臓組織とマイクロ流体チップで構成されている。マイクロ流路内の蛍光粒子の変異をモニタリングすることで、心臓組織の拍動を可視化し、ポンプ流量、圧力、力など生理的パラメーターを定量化する。これまでに報告されている心筋細胞シートの収縮力評価系と比べて、2桁高い感度で微小な力を検出できる。
マイクロ流体チップ上に装着する3次元的なマイクロ心臓組織は、まず、心筋細胞や血管の細胞など、心臓を構成する多種類の細胞をヒトiPS細胞から誘導して培養し、細胞シート状の人工心臓組織を作製した。この組織を動的トレーニング培養することで、内部に血管網を持つ厚み150〜200μmほどのマイクロ心臓組織を作製した。
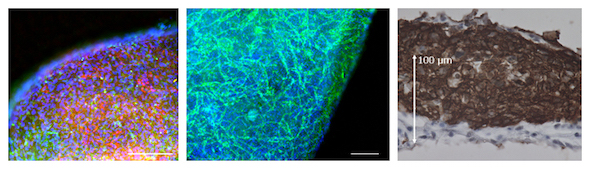 動的トレーニング培養を経て得られたヒトiPS細胞からのマイクロ心臓組織。左:心筋細胞(赤)および血管壁細胞(緑)。中央:血管内皮細胞(緑)。左と中央のスケールバーは200μm。右:心筋層(茶)(クリックで拡大) 出典:理化学研究所
動的トレーニング培養を経て得られたヒトiPS細胞からのマイクロ心臓組織。左:心筋細胞(赤)および血管壁細胞(緑)。中央:血管内皮細胞(緑)。左と中央のスケールバーは200μm。右:心筋層(茶)(クリックで拡大) 出典:理化学研究所次に、微小な電気機械システムであるMicro Electro Mechanical Systems(MEMS)技術により、シリコンの1種ジメチルポリシロキサンを用いて、マイクロ流路を作製した。この上にマイクロ心臓を載せると、拍動が流路に伝えられる仕組みで、微細な拍動を蛍光粒子の動きで可視化できる。
同マイクロデバイスの機能を検証するため、カルシウムイオンセンサータンパク質の遺伝子を導入したiPS細胞からマイクロ心臓組織を作製し、心臓の拍動と相関がある細胞内カルシウムイオンの濃度変化を観察した。その結果、カルシウムイオン濃度の振動と拍動の周波数に相関があることが確認された。
この相関は、マイクロデバイスの拍動速度の変化を反映した蛍光粒子の動きと同じであることから、今回開発したマイクロデバイスが拍動、つまり心筋細胞の活動を捉えていることが分かった。また、心筋の収縮作用を持つβ-アドレナリン受容体を作動させる薬剤、イソプロテレノールを作用させた結果からも、同デバイスが実際の心臓機能を再現していることが確認できた。
これまで、人工心臓組織の機能を高感度に評価できるシステムは確立されていなかったが、今回開発されたマイクロデバイスが、人工心臓の機能評価をはじめ、創薬や心臓毒性試験などに役立つことが期待される。
- 75秒で精子濃度など20項目を自動解析 男性不妊検査向け装置を提案
- 脳動脈瘤の治療をより安全に テルモが細径対応の新デバイス発売
- 約10秒で検温完了 ケースごと丸洗い可能なテルモの新型体温計
- 日立ら肺がん細胞診の新解析技術 SEMと元素分析で検体評価を支援
- 細胞治療の調製から充填をシステムで自動化、品質のばらつき軽減へ
- がんの微小病変解析をより正確に、1台で核酸抽出から定量を自動処理する装置
- キヤノンが医療ITをブランド統合、AI解析で新ソリューションの展開へ
- ポリエチレン9割で構成した医療用滅菌包材のサンプル提供開始
- 微小重力下での細胞解析に向け、生細胞観察装置がISSへ打ち上げ
- AIで微細デバイスを鮮明に、低被ばく低造影剤の新型X線透視装置
関連記事
 実験計画法にAIを組み合わせ、人工心臓のデザインを最適化することに成功
実験計画法にAIを組み合わせ、人工心臓のデザインを最適化することに成功
産業技術総合研究所は、実験計画法にAIの手法を組み合わせることで、少ないシミュレーション回数で人工心臓のデザインを最適化することに成功した。最適化により、同人工心臓は機能向上と副作用低下の両立が可能になっている。 化学エネルギーのみで駆動する自律型ゲルポンプの機能を実証
化学エネルギーのみで駆動する自律型ゲルポンプの機能を実証
芝浦工業大学は、電力を必要とせず化学エネルギーのみで駆動する人工心臓のようなゲルが、自律型ポンプとして機能することを証明した。ゲルのBZ反応による自発的な運動を動力源としている。 柔らかい人工筋肉のダイナミクスを用いて高精度の長さ推定に成功
柔らかい人工筋肉のダイナミクスを用いて高精度の長さ推定に成功
東京大学とブリヂストンは、空気圧アクチュエーターに基づいた人工筋肉について、人工筋肉のダイナミクスと機械学習法を組み合わせることで、加圧駆動時にリアルタイムで高精度に長さが推定できることを示した。 3Dプリント人工呼吸器の製図データを無償提供するプロジェクトが始動
3Dプリント人工呼吸器の製図データを無償提供するプロジェクトが始動
国立病院機構新潟病院と広島大学の医師を中心とする「COVIDVENTILATOR PROJECT」が始動した。3Dプリンタで容易に作製可能な人工呼吸器の製図データを、全世界に無償提供することを目指す。 新型コロナで不足する人工呼吸器の開発を支援、ルネサスが参照回路設計を公開
新型コロナで不足する人工呼吸器の開発を支援、ルネサスが参照回路設計を公開
ルネサス エレクトロニクスはオープンソースの設計仕様に基づいた移動式人工呼吸器のレファレンスデザインを作成した。人工呼吸器システムの開発短縮化につながる可能性。 違和感のない膝を再現する、人工膝関節手術支援ロボットを導入
違和感のない膝を再現する、人工膝関節手術支援ロボットを導入
慶應義塾大学病院は、赤外線誘導式人工膝関節手術支援ロボット「NAVIO」を導入した。個人の膝の状態に合わせた細やかな手術が可能で、違和感のない、安定した膝が再現できるため、患者の負担を軽減する。
関連リンク
Copyright © ITmedia, Inc. All Rights Reserved.
医療機器の記事ランキング
- 脳動脈瘤の治療をより安全に テルモが細径対応の新デバイス発売
- 75秒で精子濃度など20項目を自動解析 男性不妊検査向け装置を提案
- 知人より見知らぬ他人とシンクロ? スポーツ観戦の熱狂を科学的に解明
- 約10秒で検温完了 ケースごと丸洗い可能なテルモの新型体温計
- 抗体薬などの体内動態を追跡、数週間の長期PET撮像を実現
- 生きた乳酸菌は代謝、死んだ乳酸菌は免疫へ 状態で異なる腸内効果
- 厚さ約25μmの神経シートを開発、光刺激と記録を同時に実現
- 日立ら肺がん細胞診の新解析技術 SEMと元素分析で検体評価を支援
- 50万人の情報が流出した英国バイオバンクのインシデントでPETs利用は拡大するか
- あなたの「網膜」は実年齢より老けている? 写真1枚でAIが疾患リスクを推定
コーナーリンク

 MEMS技術により作製したマイクロ流体チップ。白い矢印がさすのは蛍光粒子を流す幅100μmの溝 出典:理化学研究所
MEMS技術により作製したマイクロ流体チップ。白い矢印がさすのは蛍光粒子を流す幅100μmの溝 出典:理化学研究所