吸入麻酔薬の作用メカニズムの一端を解明:医療技術ニュース
東京大学は、カルシウム放出チャネルの1型リアノジン受容体が、吸入麻酔薬の標的分子として全身麻酔の導入に関与していることを明らかにした。吸入麻酔薬が生体内でどのように作用し、全身麻酔を誘導するかを解明する重要な知見として期待される。
東京大学は2025年6月4日、カルシウム放出チャネルの1型リアノジン受容体(RyR1)が、吸入麻酔薬の標的分子として全身麻酔の導入に関与していることを発表した。筑波大学、順天堂大学、日本大学との共同研究によるもので、より優れた麻酔薬や投与方法への発展が期待される。
研究ではまず、RyR1や2型リアノジン受容体(RyR2)などを発現誘導できる細胞株を使用し、小胞体からカルシウム放出を検出する実験系を構築。イソフルランやクロロホルムなどの吸入麻酔薬への反応性を測定したところ、いずれもRyR1を活性化することが分かった。特にイソフルランは、RyR1を選択的に活性化していた。
次に、イソフルランに反応するRyR1と反応しないRyR2をさまざまな割合で融合させ、30種類以上のキメラ受容体を作製した。そのうち、ウサギ由来RyR1タンパク質の4000番目のアミノ酸残基メチオニンが、イソフルランの反応性に重要だと分かった。中でも、メチオニンをフェニルアラニンに置換した際に反応性が減弱していることから、分子動力学的シミュレーションによりイソフルランの結合部位を推定した。
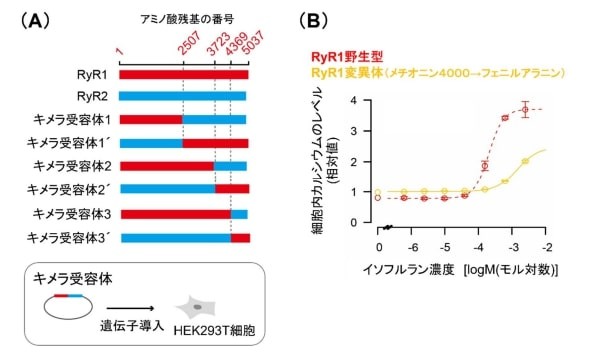 キメラ受容体の作製とイソフルラン反応性が低下した変異体の特定。(A)キメラ受容体の作製と培養細胞への遺伝子導入。(B)RyR1タンパク質の4000番目のアミノ酸(メチオニン)をフェニルアラニンに置換した変異体のイソフルラン反応性(黄色の線) 出所:東京大学
キメラ受容体の作製とイソフルラン反応性が低下した変異体の特定。(A)キメラ受容体の作製と培養細胞への遺伝子導入。(B)RyR1タンパク質の4000番目のアミノ酸(メチオニン)をフェニルアラニンに置換した変異体のイソフルラン反応性(黄色の線) 出所:東京大学イソフルランへの反応性を失ったRyR1を発現するノックインマウスでは、正常なマウスよりもイソフルランに対する感受性が部分的に低下し、麻酔にかかりづらくなった。また、推定したイソフルランの結合部位に作用する新規化合物を特定してマウスに投与したところ、脳波の変化を伴う鎮静作用に近い効果が見られ、イソフルランに対する感受性が高まった。これらの結果から、RyR1がイソフルランの標的分子として、マウスの麻酔作用に関与することが示唆された。
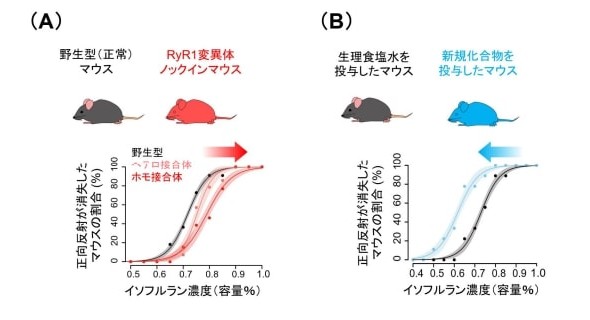 イソフルラン麻酔による正向反射(自然な睡眠では保たれるが、全身麻酔では消失する運動反射)消失の変化。(A)イソフルランに対する感受性が減弱したRyR1変異体を発現するノックインマウスの正向反射消失(n=11-14)。(B)イソフルランの推定結合部位に作用する新規化合物を投与したマウスの正向反射消失(n=9) 出所:東京大学
イソフルラン麻酔による正向反射(自然な睡眠では保たれるが、全身麻酔では消失する運動反射)消失の変化。(A)イソフルランに対する感受性が減弱したRyR1変異体を発現するノックインマウスの正向反射消失(n=11-14)。(B)イソフルランの推定結合部位に作用する新規化合物を投与したマウスの正向反射消失(n=9) 出所:東京大学今回の成果は、吸入麻酔薬の分子メカニズムの一端を明らかにするものとなる。生体内でどのように作用し、全身麻酔を誘導するかを解明する重要な知見になるとしている。
関連記事
 薬剤を2000倍に濃縮して内包できる無機ナノ粒子カプセル作製法を確立
薬剤を2000倍に濃縮して内包できる無機ナノ粒子カプセル作製法を確立
北海道大学らは、無機ナノ粒子を構成要素としたナノサイズの中空カプセル構造体作製技術を開発した。薬剤を2000倍以上に濃縮して効率的に内包できるため、次世代の薬物送達キャリアとして期待される。 血液から直接神経細胞を生み出す技術を開発
血液から直接神経細胞を生み出す技術を開発
慶應義塾大学と藤田医科大学は、末梢血細胞からiPS細胞への初期化を介さずに神経細胞を産生する技術を開発した。誘導前の細胞が保有していた情報の一部を受け継ぐ神経細胞が、遺伝子導入から約20日で産生する。 再起動したトランプ政権の公的医療保険改革とデジタルヘルス
再起動したトランプ政権の公的医療保険改革とデジタルヘルス
本連載第111回で取り上げたように、米国の臨床現場における医療データ流通やAI利用を支えてきたデジタルヘルスは、第2次トランプ政権における公的医療保険改革ツールとして再起動した。 協業契約に基づき、産婦人科向け超音波診断装置の新製品を発売
協業契約に基づき、産婦人科向け超音波診断装置の新製品を発売
キヤノンメディカルシステムズとコニカミノルタは、両社の販売基本協業契約において取り扱う新製品として、女性診療に特化した超音波診断装置「Aplio beyond/Women's Healthモデル」を発売した。 焦点深度を拡張した白内障治療向け非回折多焦点眼内レンズを発売
焦点深度を拡張した白内障治療向け非回折多焦点眼内レンズを発売
Johnson&Johnsonは、遠方から近方距離まで焦点深度を拡張した、非回折焦点深度拡張型眼内レンズ「テクニス ピュアシー」を国内で発売する。白内障手術用多焦点眼内レンズの新しい選択肢の1つとなる。 患者の投稿画像からアトピー性皮膚炎の重症度を解析するAIモデル
患者の投稿画像からアトピー性皮膚炎の重症度を解析するAIモデル
慶應義塾大学と帝京大学は、アトピー性皮膚炎患者向け投稿アプリを用いて、患者自身が撮影した皮疹画像から重症度をAIが自動で解析、評価するAIモデルを開発した。
関連リンク
Copyright © ITmedia, Inc. All Rights Reserved.
医療機器の記事ランキング
- 脳動脈瘤の治療をより安全に テルモが細径対応の新デバイス発売
- 約10秒で検温完了 ケースごと丸洗い可能なテルモの新型体温計
- 厚さ約25μmの神経シートを開発、光刺激と記録を同時に実現
- 知人より見知らぬ他人とシンクロ? スポーツ観戦の熱狂を科学的に解明
- 生きた乳酸菌は代謝、死んだ乳酸菌は免疫へ 状態で異なる腸内効果
- 日立ら肺がん細胞診の新解析技術 SEMと元素分析で検体評価を支援
- あなたの「網膜」は実年齢より老けている? 写真1枚でAIが疾患リスクを推定
- 50万人の情報が流出した英国バイオバンクのインシデントでPETs利用は拡大するか
- がんの微小病変解析をより正確に、1台で核酸抽出から定量を自動処理する装置
- 猛暑の夏を乗り切る! 冷却性能20%増の首元デバイスで−2℃体験へ
コーナーリンク
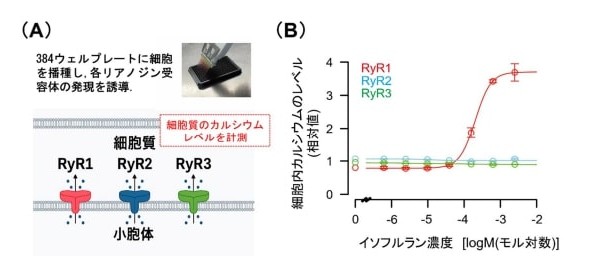 カルシウム放出の検出実験概要図とイソフルランによるRyR1の活性化 出所:東京大学
カルシウム放出の検出実験概要図とイソフルランによるRyR1の活性化 出所:東京大学


