さまざまな反応器における設計方程式:はじめての化学工学(11)(2/2 ページ)
PFRの設計方程式
PFRは流体が管出口に近づくほど反応が進みます。そのため原料Aの消費速度は、管内における位置を表す体積座標V(もしくは長さ)の変化から求められます。CSTRと同様に、反応速度式を組み合わせることで、空間時間を用いた式表現が出来ます。
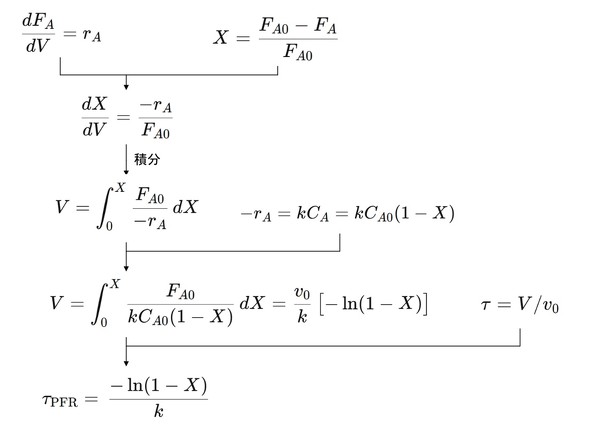 図6 一次不可逆反応におけるPFRの設計方程式。FA:反応後のモル流量、FA0:反応後のモル流量、V:体積、v0:体積流量、X:転化率、rA:原料Aの消費速度、k:反応速度定数、T:空間時間[クリックで拡大]
図6 一次不可逆反応におけるPFRの設計方程式。FA:反応後のモル流量、FA0:反応後のモル流量、V:体積、v0:体積流量、X:転化率、rA:原料Aの消費速度、k:反応速度定数、T:空間時間[クリックで拡大]実は、この式はBRの結果と一致します。つまりBRでの反応時間とPFRでの空間時間が同じ式形です。
CSTRとPFRの特性比較
同じ連続式であるCSTRとPFRについて、求めた空間時間空特性を比較します。空間時間Tは(体積)/(体積流量)=V/v0であるため、値が小さい方が反応器のサイズを小さくできます。
式から、PFRの方がCSTRよりも小さい体積で反応できます。この影響は高い転化率を求めるほど顕著に現れます。反応速度定数k=0.20s-1とし、転化率X=0.50と0.90の2種類で比較します。X=0.50のとき、TPFR=3.5s、TCSTR=5.0sです。対してX=0.90のとき、TPFR=12s、TCSTR=45sです。
PFRの反応は、入り口で高濃度/高速度で一気に進みます。対してCSTRの反応は、混合で常に希釈された状態で行われます。反応時間の面ではPFRの方が有利です。しかしPFRは急激に反応が進むことから、反応熱により温度が急上昇することも意味します。局所的な温度上昇を防ぐ必要があり、反応熱の除去難易度が向上します。
CSTRの出口に次のCSTRを設けるように、直列多段に接続したとします。すると各段で原料の出口濃度が階段状に下がりながら反応は進みます。段数を増やすほど階段は滑らかになり、軸方向で連続的に濃度が変わるPFRの挙動に近づきます。
ただし、段数を増やすほど転化率は上がりますが、次第に効果は薄れていきます。装置規模(体積/コスト)を抑えつつPFRに近づける現実的な解は、5〜10段程度です。実際に転化率をPFR並みにするには数十段の構成が求められてしまい、現実的ではありません。体積(コスト)、選択性(品質)、除熱(安全性)を加味して総合的に設備構成を決定します。
まとめ
今回は転化率と空間時間の視点から、各反応器の設計方程式を紹介しました。この考え方が基本となります。そして今回取り上げた一次、不可逆、等温という条件からさらに反応条件を広げていくことでさまざまな反応に対応できるようになります。(次回へ続く)
関連記事
 反応装置の種類と反応特性
反応装置の種類と反応特性
化学プラントで用いられる反応装置は、その操作方式や構造によって異なる反応特性を示します。代表的な反応装置ごとに基本構造と特徴を解説します。 撹拌動力計算とスケールアップ指標
撹拌動力計算とスケールアップ指標
前回は、撹拌の概念や装置について解説しました。今回は、撹拌槽の設計や運転条件を決める上で欠かせない撹拌動力計算と無次元指標、スケールアップの考え方について解説します。 撹拌の役割と基本構成
撹拌の役割と基本構成
撹拌は化学プロセスを安定/高効率に運転する上で不可欠な単位操作です。今回は撹拌の役割や装置構成について、そして撹拌翼の種類について解説します。 化学プロセスにおけるバッチ操作と連続操作の違い
化学プロセスにおけるバッチ操作と連続操作の違い
化学プロセスは大きくバッチ操作と連続操作に分類されます。これらは製造する製品の特徴や品質要件にあった操作が選択されます。今回はバッチ操作と連続操作の一般的な違いと使い分け方を紹介します。 物質収支とエネルギー収支の考え方
物質収支とエネルギー収支の考え方
化学工学計算の中で物質収支とエネルギー収支は、化学プロセスの挙動を理解し最適化するために不可欠です。今回は、物質収支やエネルギー収支の基本的な考え方と計算事例を解説します。 配管流れの基本的な計算方法
配管流れの基本的な計算方法
化学プラントでは、原料や製品、中間生成物などさまざまな流体を目的の場所に輸送する必要があります。それぞれの単位操作の間は配管をつないで移送されることから、配管はプラントの血管とも言えます。今回は配管設計の基本となる事項を解説します。 そもそも化学工学って何?
そもそも化学工学って何?
化学工学は、多くの工業製品の生産を陰で支える重要な学問分野です。しかし、化学工学とは具体的に何をするのでしょうか? 第1回は、初めて化学工学を学ぶ方を対象に基本的な要素を分かりやすく解説します。 実験室で成功した化学反応を工業規模で再現する難しさとは?
実験室で成功した化学反応を工業規模で再現する難しさとは?
化学工学は、実験室規模で確立した化学的プロセスを産業規模で実現するための工学分野です。規模が大きくなると不都合が生じやすく、ビーカーやフラスコとは異なる工業的に最適化された構造をしています。今回はプラントの主要な構成要素である槽、塔、熱交換器を紹介します。 コスモの製油所デジタルプラント化 三現主義を解消する技術とは?
コスモの製油所デジタルプラント化 三現主義を解消する技術とは?
コスモエネルギーグループに、製油所のデジタルプラント化の背景や特徴、導入による大きな利点、今後の展開について聞いた。 合成樹脂製造プラントの運転自動化を実現するデジタルツイン技術を実用化
合成樹脂製造プラントの運転自動化を実現するデジタルツイン技術を実用化
DICと日立製作所は、合成樹脂製造プラントの運転自動化を図るデジタルツイン技術として、プロセスインフォマティクスを活用したシステムを実用化し、DICの国内プラントで2025年1月に本格稼働する。 NEC、大規模ボイラープラントでAIによる運転支援システムの実証実験に成功
NEC、大規模ボイラープラントでAIによる運転支援システムの実証実験に成功
NECは、化学プラントなどの運転を支援する「プラント運転支援AI」と、シミュレーター上に再現したミラープラントを組み合わせたプラント運転支援システムを構築し、井化学大阪工場の大規模ボイラープラントでの実証実験に成功した。
関連リンク
Copyright © ITmedia, Inc. All Rights Reserved.
コーナーリンク





