体温維持に必要な寒冷感知タンパク質のリン酸化と遺伝子の立体構造:医療技術ニュース
東京大学は、寒冷時に熱産生遺伝子の発現を急速に活性化して体温を維持するには、熱産生をつかさどる遺伝子DNA(クロマチン)の急速な立体構造変化が必須であることを解明したと発表した。
東京大学は2015年5月15日、寒冷時に熱産生遺伝子の発現を急速に活性化して体温を維持するには、「転写因子」と呼ばれるタンパク質群の働きだけではなく、熱産生をつかさどる遺伝子DNA(クロマチン)の急速な立体構造変化が必須であることを解明したと発表した。同研究は、同大先端科学技術研究センター代謝医学分野の酒井寿郎教授、稲垣毅特任准教授、阿部陽平特任研究員らの研究グループによるもの。
ヒトや哺乳動物は、体が寒冷環境に置かれると中枢でこれを感知し、交感神経からの刺激によって、熱産生を専門に行う褐色脂肪組織で迅速に熱が産生され、低体温になることを防ぐ。同研究グループはこれまで、核内で遺伝子DNAのメチル基を除去するJMJD1Aタンパク質を欠損したマウスが低体温に陥ることを明らかにしていたが、その仕組みは分かっていなかった。
同研究ではまず、質量分析解析から、交感神経から寒冷刺激を受けた核内のタンパク質「JMJD1A」の265番目のセリン残基がリン酸化されることを発見した。このアミノ酸をアラニンに置換し、リン酸化されない変異体JMJD1Aを褐色脂肪細胞に発現させると、寒冷刺激で誘導される熱産生遺伝子群の発現誘導が著しく低下し、褐色脂肪細胞での熱産生が低下した。
さらに、質量分析解析から、このリン酸化が引き金となって、「遺伝子の高次構造を変化させる複数のタンパク質群(SWI/SNF)」や「褐色脂肪細胞の機能に重要な核内受容体(PPARγ)」と複合体を形成することが分かった。この複合体が、「長距離DNAルーピング」と呼ばれる遺伝子の高次構造変化を起こすことで、熱産生・エネルギー消費
を制御していることが分かった。これら一連の変化は、数分から十数分の速さで起こり、熱産性に関わる遺伝子の発現を急速に促すという。
同研究成果は、JMJD1Aタンパク質を標的とした、低体温症や熱産生・エネルギー消費が低下して起こる肥満のための新規治療法や予防法にもつながるとしている。
なお、同研究は、2015年5月7日に国際科学誌「Nature Communications」オンライン版に掲載された。
- 知人より見知らぬ他人とシンクロ? スポーツ観戦の熱狂を科学的に解明
- 厚さ約25μmの神経シートを開発、光刺激と記録を同時に実現
- 生きた乳酸菌は代謝、死んだ乳酸菌は免疫へ 状態で異なる腸内効果
- あなたの「網膜」は実年齢より老けている? 写真1枚でAIが疾患リスクを推定
- 50万人の情報が流出した英国バイオバンクのインシデントでPETs利用は拡大するか
- ミカンの1種“タチバナ”にシミ抑制効果、メラニンの蓄積を阻害
- セラミド不足がアトピー性皮膚炎の直接原因であることを実証
- エッジAI搭載の前眼部検査機で白内障など早期発見へ、従来機より低コスト化も
- 外科医と対話する生成AI、胃がん手術の実証実験で有用性80%達成
- 医療機器大手ストライカーの事例に見る米国サイバーインシデント情報開示の複雑性
関連記事
 チェス、オセロ、クイズの次は「東大」だ!! ――NII「人工頭脳プロジェクト」始動
チェス、オセロ、クイズの次は「東大」だ!! ――NII「人工頭脳プロジェクト」始動
国立情報学研究所の人工頭脳プロジェクトは「ロボットは東大に入れるか」というグランドチャレンジに向け始動。2016年までに大学入試センター試験で高得点をマーク、2021年に東京大学入試を突破を目指す。 運転能力を低下させる白質病変、東京大学らが実車実験で確認
運転能力を低下させる白質病変、東京大学らが実車実験で確認
東京大学と高知工科大学は、医学的に症状のない軽度の大脳白質病変(以下、白質病変)と診断された高齢の運転者は、そうでない高齢の運転者に比べて、運転能力が低下していることが実車実験で確認できた、と発表した。 「超小型衛星の世界を変える!!」――世界最小クラスのイオンエンジン「MIPS」
「超小型衛星の世界を変える!!」――世界最小クラスのイオンエンジン「MIPS」
東京大学 先端科学技術研究センターの小泉宏之准教授と次世代宇宙システム技術研究組合(NESTRA)が共同開発している世界最小クラスのイオンエンジン「MIPS」。このMIPSとは一体どのようなエンジンなのか、これにより超小型衛星の世界がどのように変わるのか。開発者に聞く。 3Dデザイン/設計スキルを学ぶ世界イベントに東大生3人が日本代表として参加
3Dデザイン/設計スキルを学ぶ世界イベントに東大生3人が日本代表として参加
オートデスクは、製造や建築分野の3Dデザイン/設計スキルの集中トレーニングを行うワールドワイドの学生向けイベント「Autodesk Panorama」の日本代表として、東京大学の学生3人が選ばれたと発表した。 「はやい」だけではダメ! 今までにないものを作ってこそ3Dプリンタは意味がある
「はやい」だけではダメ! 今までにないものを作ってこそ3Dプリンタは意味がある
工作機械と関連製品/技術の展示会「第27回日本国際工作機械見本市(JIMTOF 2014)」の基調講演として東京大学 生産技術研究所 教授の新野俊樹氏が登壇。「Additive Manufacturingを核にした新しいモノづくり――3Dプリンタの未来像」をテーマに付加製造技術の発展の歴史と今後の課題について語った。
関連リンク
Copyright © ITmedia, Inc. All Rights Reserved.
医療機器の記事ランキング
- 脳動脈瘤の治療をより安全に テルモが細径対応の新デバイス発売
- 約10秒で検温完了 ケースごと丸洗い可能なテルモの新型体温計
- 厚さ約25μmの神経シートを開発、光刺激と記録を同時に実現
- 知人より見知らぬ他人とシンクロ? スポーツ観戦の熱狂を科学的に解明
- 生きた乳酸菌は代謝、死んだ乳酸菌は免疫へ 状態で異なる腸内効果
- 日立ら肺がん細胞診の新解析技術 SEMと元素分析で検体評価を支援
- あなたの「網膜」は実年齢より老けている? 写真1枚でAIが疾患リスクを推定
- 50万人の情報が流出した英国バイオバンクのインシデントでPETs利用は拡大するか
- 75秒で精子濃度など20項目を自動解析 男性不妊検査向け装置を提案
- がんの微小病変解析をより正確に、1台で核酸抽出から定量を自動処理する装置
コーナーリンク
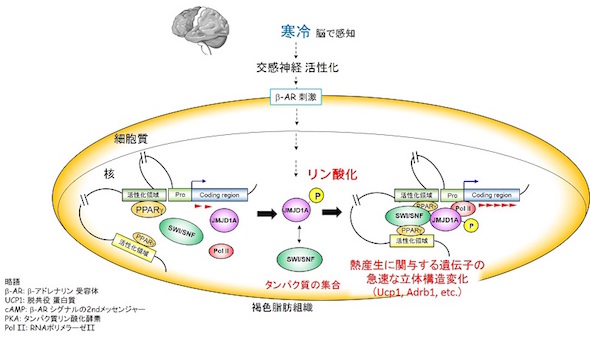 寒冷刺激によって褐色脂肪細胞の熱産生遺伝子が急速に活性化される、DNAの高次構造変化を介した新たなしくみ
寒冷刺激によって褐色脂肪細胞の熱産生遺伝子が急速に活性化される、DNAの高次構造変化を介した新たなしくみ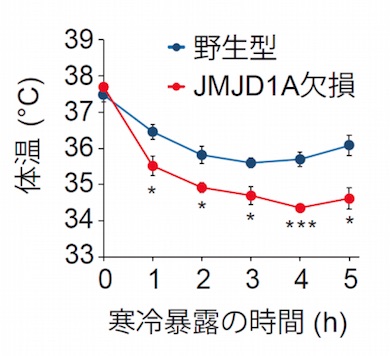 寒冷刺激によるマウスの体温の変化
寒冷刺激によるマウスの体温の変化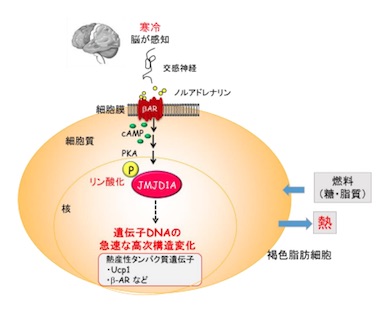 褐色脂肪細胞における寒冷刺激による急速な熱産生遺伝子誘導のしくみ
褐色脂肪細胞における寒冷刺激による急速な熱産生遺伝子誘導のしくみ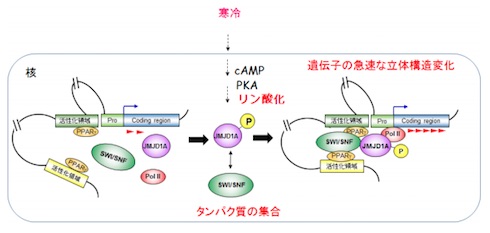 遺伝子の急速な立体構造変化
遺伝子の急速な立体構造変化


