リチウムイオンが充放電に関与すれば、どんな材料でも「リチウムイオン電池」!?:今こそ知りたい電池のあれこれ(3)(1/2 ページ)
そもそもこの「リチウムイオン電池」とは、どんな電池でしょうか? この質問、単純に見えて実は意外と厄介なものです。
これまで本コラムではリチウムイオン電池の安全性について、「なぜ膨張するのか」、「なぜ発熱・発火するのか」といった解説をしてきました。ところで、そもそもこの「リチウムイオン電池」とは、どんな電池でしょうか? この質問、単純に見えて実は意外と厄介なものです。
NHKの人気番組「チコちゃんに叱られる!」(2020年3月13日放送回)でも、「リチウムイオン電池ってなに?」という問い掛けがありましたが、あのチコちゃんでさえ「一言では言えないのでノーベル賞受賞者吉野彰さんが1時間かけて分かりやすく説明してくれました」と回答したほどです。
また、本コラム第1回において、私自身も以下のように述べました。
実は「リチウムイオン電池」というのは非常に懐の深い名称であり、材料構成や電池特性が大きく異なるものであったとしても全て一緒くたにして「リチウムイオン電池」と呼ぶことができてしまいます。
今や身の回りのさまざまな場所に用いられている「リチウムイオン電池」ですが、正しく理解するのはなかなか難しい技術でもあります。チコちゃんに「ボーっと生きてんじゃねーよ!」と叱られないためにも、そもそもリチウムイオン電池とは何なのか、どのようにして私たちの生活に貢献してきたのかを解説したいと思います。
リチウムイオン電池は多種多様
「リチウムイオン電池ってなに?」という問い掛けに、私が一言で答えるとするならば、少々硬い言い回しをすると「リチウムイオンを電荷担体(キャリア)とする二次電池の総称」となります。言い換えると「充電・放電にあわせてリチウムイオンが正極と負極の間を行ったり来たりすることで繰り返し使うことができる電池」です。
ここで大事なのは、この回答には「具体的な材料の情報が含まれていない」ということです。例えば、マンガン乾電池は「正極に二酸化マンガン、負極に亜鉛を用いた(使い捨ての)一次電池」です。ニッケル水素電池であれば「正極にニッケル酸化化合物、負極に水素または水素化合物を用いた(充電して再利用可の)二次電池」という具合に、他の電池系の場合はその名称が使用される材料と結び付いており、ある程度は具体的な反応系を限定することができます。
一方、リチウムイオン電池の場合は先述の通り、あくまでも「充放電にリチウムイオンが関与する二次電池の総称」でしかなく、たとえどんな材料を使っていても、どんな構造で、どんな電池特性であったとしても、全て「リチウムイオン電池」と呼ぶことができてしまいます。
それだけ多種多様な構成が考えられるリチウムイオン電池ですが、具体的にどのような材料が使用され、それぞれどんな特徴があるのかについては、詳細を述べていくと、とても長い話になってしまいますので、あらためて別の回で解説します。
一般的な材料構成に限って考えた場合、リチウムイオン電池の狭義な定義は「正極にリチウムイオン含有金属酸化物(LiCoO2等)、負極にカーボン材料を用いた非水系電解液二次電池」といえます。
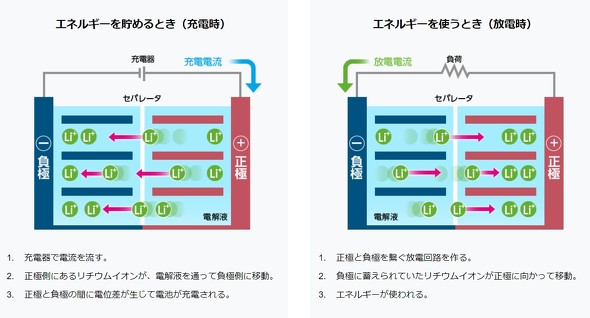
正極のリチウムイオン含有金属酸化物中に存在するリチウムイオンが、充電によって負極のカーボン材料の中へ、逆に放電によって負極のカーボン材料の外へと移動し、充電/放電にあわせてリチウムイオンが正極と負極の間を行ったり来たりすることが基本の電池反応となっています。下記が一般的なリチウムイオン電池の反応式の例です。
正極:Li(1-x)CoO2+xLi++xe-←→LiCoO2
負極:LixC←→C+xLi++xe-
電池全体:Li(1-x)CoO2+LixC←→LiCoO2+C
正極の「リチウムイオン含有金属酸化物」、負極の「カーボン材料」のように、電池の容量を担う材料のことを活物質といいます。この活物質だけでは電極にはならず、電極抵抗を削減するための導電助剤、他の材料とのつなぎや結着を担うバインダーといった材料との混合物を金属箔に担持したものが、リチウムイオン電池の電極として用いられています。
水系電解液から非水系電解液に
リチウムイオン電池の重要な特徴の1つは「金属リチウム」ではなく「リチウムイオン」が反応に寄与するという点です。化学的に不安定な金属リチウムが不要となることで電池としての安全性が向上し、広く普及する一因となりました。
もう1つの重要な特徴は「4V以上の高い起電力」を有するという点です。充電して再利用可能な電池の中でも、鉛蓄電池やニカド電池、ニッケル水素電池などは水系の電解液を用いた電池です。水は電解質塩の溶解性やイオンの移動度といった観点からは電解液に適した溶媒ですが、約1.5V以上の電圧がかかると水素と酸素に電気分解してしまうため、これらの電池の起電力を高くするには限界がありました。
リチウムイオン電池の場合、炭酸エステル系の有機溶媒にLiPF6などのリチウム塩を溶解した非水系電解液を使用することで、水系電解液よりも高電圧耐性が向上しました。これによって、リチウムイオン電池は従来の水系電解液の電池よりもエネルギー密度を高め、小型で軽量な電池とすることができました。こうした安全性の向上や、小型・軽量化がリチウムイオン電池の普及につながっています。
Copyright © ITmedia, Inc. All Rights Reserved.
モビリティの記事ランキング
- 新型「bZ4X」の走行距離が伸びた理由、デンソーの「世界初」と「世界最高」が貢献
- ギガキャストを発案したテスラの現在・過去・未来
- ECUの一体化で進化したトヨタの「新型TSS」 RAV4の安全走行を支える技術とは
- スズキ、排出ガス中のCO2を回収し農場で再利用できる「スーパーキャリイ」披露
- どこへでも移動可能な自由を── ランドクルーザーの新型車「FJ」シリーズが登場
- 「新興勢力に圧倒的に劣っている」――ホンダは開発を根本から変えられるか
- 新型「CX-5」はSUVの王道を極める、SDV化も進みアップデートでGeminiも利用可能
- 4kWhバッテリー搭載電動バイク「L-noa」 大手4社に原付一種で挑む理由
- コマツが次世代月面物流ローバーの研究開発を開始
- SDV時代には「製品開発スピード」だけでなく「製品発見スピード」も求められる
コーナーリンク