染色体にアセチル化加飾を行うシステムを開発、がん抑制遺伝子の転写促進:医療技術ニュース
東京大学は、染色体タンパク質に対して、アセチル化修飾を選択的に行う人工化学触媒システム「SynCAcシステム」を開発した。このシステムを用いることで、遺伝子の転写を人工的に促進できる可能性が示唆された。
東京大学は2017年6月11日、染色体タンパク質に対して、アセチル化修飾を選択的に行う人工化学触媒システム「SynCAcシステム」を開発したと発表した。さらに、同システムを用いることで、遺伝子転写を人工的に促進する可能性が示唆された。同大学大学院 薬学系研究科 教授の金井求氏、特任講師の川島茂裕氏、助教の山次健三氏らのグループによるもので、成果は6月8日、米化学誌「Chem」オンライン速報版で公開された。
今後、SynCAcシステムは、生体内反応の機能を解明する実験技術の開発につながることが期待される。また、生体内に人工化学触媒システムを導入し、人工的にヒストンのアセチル化修飾が可能になると、触媒医療としてがん/リンパ腫などさまざまな疾患の治療につながる可能性があるという。
染色体の最小単位は、ヒストンと呼ばれるタンパク質とDNAの複合体ヌクレオソームから構成される。DNAに保存されている遺伝情報は転写を経て、最終的にタンパク質に変換されることで発現する。ヒストンは酵素によってさまざまな化学修飾を受け、それによって遺伝子の転写が促進/抑制される。特にアセチル化修飾は、がん抑制遺伝子などの転写を促進することが知られている。
同研究グループは、DNAを認識してヌクレオソームに結合する触媒とアセチル化剤を組み合わせ、ヌクレオソームと反応させることを考えた。そこで、DNAが負の電荷性を帯びている性質を利用し、正の電荷性を持つ触媒とアセチル化剤を設計。これらをSynCAcシステムにより同時に用いて、生体内の酵素を介さずにヒストンを人工的にアセチル化修飾することに成功した。また、さまざまなタンパク質が混在する中でもヒストン選択的にアセチル化が進行した。
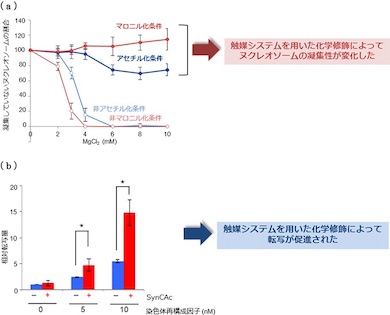
未修飾のヌクレオソームは高濃度のマグネシウムイオン存在下で凝集するが、今回アセチル化修飾を行ったヌクレオソームは、高濃度のマグネシウムイオン存在下でも凝集が抑えられていた。また、このアセチル化が染色体再構成因子の存在下で転写を促進することを発見した。これらは、人工の化学触媒システムが生体内の酵素と同等の機能を示し得るということを示唆している。
さらに、アセチル化剤をマロニル化剤に変えるとマロニル化反応が進行し、ヌクレオソームの性質が大きく変化することも明らかになった。
- 知人より見知らぬ他人とシンクロ? スポーツ観戦の熱狂を科学的に解明
- 厚さ約25μmの神経シートを開発、光刺激と記録を同時に実現
- 生きた乳酸菌は代謝、死んだ乳酸菌は免疫へ 状態で異なる腸内効果
- あなたの「網膜」は実年齢より老けている? 写真1枚でAIが疾患リスクを推定
- 50万人の情報が流出した英国バイオバンクのインシデントでPETs利用は拡大するか
- ミカンの1種“タチバナ”にシミ抑制効果、メラニンの蓄積を阻害
- セラミド不足がアトピー性皮膚炎の直接原因であることを実証
- エッジAI搭載の前眼部検査機で白内障など早期発見へ、従来機より低コスト化も
- 外科医と対話する生成AI、胃がん手術の実証実験で有用性80%達成
- 医療機器大手ストライカーの事例に見る米国サイバーインシデント情報開示の複雑性
関連記事
 脳や行動の性差を決める遺伝子のスイッチを発見
脳や行動の性差を決める遺伝子のスイッチを発見
東北大学は、ショウジョウバエの実験により、脳と行動の雌雄による劇的な違いが、たった1つの遺伝子のスイッチを入れるか、切るかで生み出されることを立証した。 川崎病の発症に関わる「ORAI1遺伝子の多型」を発見
川崎病の発症に関わる「ORAI1遺伝子の多型」を発見
理化学研究所は、川崎病の発症に関わる「ORAI1遺伝子」の遺伝子多型を発見したと発表した。ORAI1タンパク質を構成するアミノ酸配列の変化に関わる一塩基多型(SNP)が川崎病と関連し、最もその頻度が高いのは日本人であることが分かった。 ヒトのウイルス糖尿病リスク遺伝子を発見
ヒトのウイルス糖尿病リスク遺伝子を発見
九州大学大学院医学研究院の永淵正法教授は、ヒトのウイルス糖尿病リスク遺伝子を同定した。ヒトTYK2遺伝子多型が、広く糖尿病の発症リスクとなり、特にウイルス感染後に1型糖尿病にかかるリスクが高いことが分かった。 熱帯感染症診断に適した遺伝子検査システムの共同研究を開始
熱帯感染症診断に適した遺伝子検査システムの共同研究を開始
長崎大学は、熱帯感染症や新興・再興感染症を対象にした新たな遺伝子検査システムの開発について、東芝メディカルシステムズと共同研究契約を締結した。2016年8月から2年間、共同研究に取り組む。 臨床現場での即時検査が可能な遺伝子検査機器
臨床現場での即時検査が可能な遺伝子検査機器
ロシュ・ダイアグノスティックスは、臨床現場で即時に検査できる遺伝子検査機器「コバス Liat」を「JACLaS EXPO 2016」に出展した。2017年に発売予定としている。
関連リンク
Copyright © ITmedia, Inc. All Rights Reserved.
医療機器の記事ランキング
- 脳動脈瘤の治療をより安全に テルモが細径対応の新デバイス発売
- 知人より見知らぬ他人とシンクロ? スポーツ観戦の熱狂を科学的に解明
- 75秒で精子濃度など20項目を自動解析 男性不妊検査向け装置を提案
- 約10秒で検温完了 ケースごと丸洗い可能なテルモの新型体温計
- 厚さ約25μmの神経シートを開発、光刺激と記録を同時に実現
- 生きた乳酸菌は代謝、死んだ乳酸菌は免疫へ 状態で異なる腸内効果
- 日立ら肺がん細胞診の新解析技術 SEMと元素分析で検体評価を支援
- 50万人の情報が流出した英国バイオバンクのインシデントでPETs利用は拡大するか
- 抗体薬などの体内動態を追跡、数週間の長期PET撮像を実現
- あなたの「網膜」は実年齢より老けている? 写真1枚でAIが疾患リスクを推定
コーナーリンク
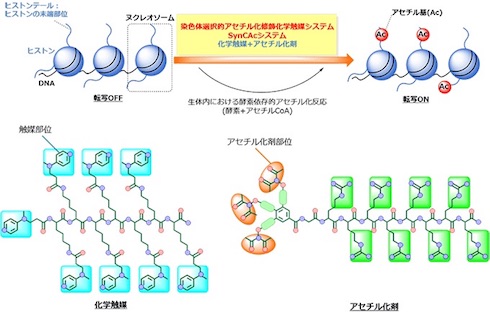
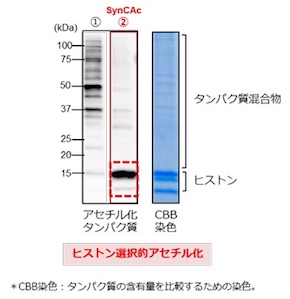 SynCAcシステムによるヒストン選択的なアセチル化 出典:東京大学
SynCAcシステムによるヒストン選択的なアセチル化 出典:東京大学