海外で進む医療ソフトウェア臨床評価の標準化:海外医療技術トレンド(20)(1/2 ページ)
日本では、2014年11月の医薬品・医療機器等法施行により、スタンドアロン製品として承認申請や市販後対策の対象となった医療ソフトウェア。海外では、国境を越えた国際標準化への取り組みが着々と進んでいる。
FDAが公開した「SaMD」の臨床評価ガイドライン草案
本連載第8回および第13回で、米国連邦取引委員会(FTC)主導で進む「非医療機器」の規制動向を取り上げたが、食品医薬品局(FDA)が所管する「医療機器」に該当するソフトウェアでは、標準化、国際協調に向けた動きが進んでいる。
2016年10月14日、米国FDAは、「ソフトウェア・アズ・ア・メディカル・デバイス(SaMD):臨床評価」と題するガイドライン草案を公開し、パブリックコメントの募集を開始した(関連情報、PDFファイル。同草案はもともと、国際医療機器規制当局フォーラム(IMDRF)のSaMDワーキング・グループが、欧州のアプローチに従い、スタンドアロンのソフトウェアを医療機器として規制するためのルールをとりまとめて、2015年8月に公開したものだ。
これに先立ってIMDRFは、2014年9月18日に公開した「ソフトウェア・アズ・ア・メディカル・デバイス:リスク分類と対応の考慮事項」(関連情報、PDFファイル)の中で、SaMDについて、1つもしくは複数の医療目的のために使用することを意図とするソフトウェアで、ハードウェア医療機器の一部となることなくこれらの目的を達成するものと定義している。
その上で、表1に示すようなSaMDの分類を提示している。医療場面や病態の現状の観点から、「危機的(Critical)」「深刻(Serious)」「深刻でない(Non-serious)」の3分類と、医療上の決定に対するSaMD提供情報の意義の観点から「治療または診断(Treat or Diagnose)」「臨床管理の運用(Drive clinical management)」「臨床管理に関する情報提供(Inform clinical management)」の3分類によるマトリックス表を提示した上で、クラスI(一般医療機器)、クラスII(管理医療機器)、クラスIII(第三者登録機関による認証が必要な高度管理医療機器)、クラスIV(規制当局による承認が必要な高度管理医療機器)のどれに該当するかを示している。
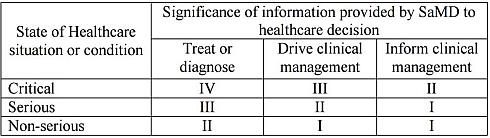 表1 国際医療機器規制当局フォーラム(IMDRF)の「Software as a Medical Service(SaMD)」分類(クリックで拡大) 出典:IMDRF「“Software as a Medical Device”: Possible Framework for Risk Categorization and Corresponding Consideration」(2014年9月18日)
表1 国際医療機器規制当局フォーラム(IMDRF)の「Software as a Medical Service(SaMD)」分類(クリックで拡大) 出典:IMDRF「“Software as a Medical Device”: Possible Framework for Risk Categorization and Corresponding Consideration」(2014年9月18日)これに対して、図1は、今回FDAが公開したガイドライン草案で示されたSaMD臨床評価上の分類を提示している。表1と比較して、一歩踏み込んだ表現になっていることが分かるだろう。
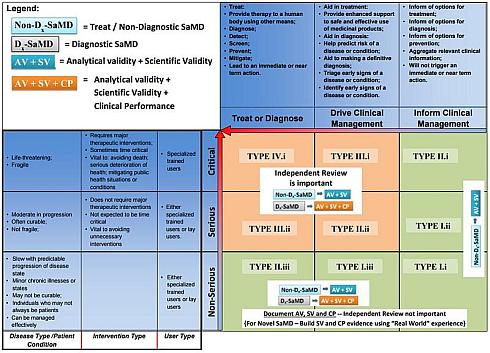 図1 SaMDの臨床評価ガイドライン草案における分類(クリックで拡大) 出典:FDA「Draft Guidance: Software as a Medical Device (SaMD): Clinical Evaluation」(2016年10月14日)
図1 SaMDの臨床評価ガイドライン草案における分類(クリックで拡大) 出典:FDA「Draft Guidance: Software as a Medical Device (SaMD): Clinical Evaluation」(2016年10月14日)本草案は、個別の最新ソフトウェア製品について、特定の要求事項を説明したものではなく、医療ソフトウェアの複雑性の下で、いかに臨床評価するかについて考慮するための一般的なフレームワークを提供したものだ。
スタンドアロンのソフトウェアも、ハードウェア医療機器に付属するソフトウェアも、臨床評価の目的は同じだが、複雑に相互接続されたオープンな環境下で稼働し、迅速かつ効率的に変更や修正を行うことが可能なソフトウェアが登場してきたことが、今回の草案策定の背景にある。日本の規制当局もIMDRFに加盟しているので、表1と図1に示されたSaMDの分類の差分を、今後、現行の医薬品医療機器等法および関連規則、ガイドライン類に反映させることが必要となるだろう。
Copyright © ITmedia, Inc. All Rights Reserved.
医療機器の記事ランキング
- 脳動脈瘤の治療をより安全に テルモが細径対応の新デバイス発売
- 約10秒で検温完了 ケースごと丸洗い可能なテルモの新型体温計
- 厚さ約25μmの神経シートを開発、光刺激と記録を同時に実現
- 知人より見知らぬ他人とシンクロ? スポーツ観戦の熱狂を科学的に解明
- 生きた乳酸菌は代謝、死んだ乳酸菌は免疫へ 状態で異なる腸内効果
- 日立ら肺がん細胞診の新解析技術 SEMと元素分析で検体評価を支援
- あなたの「網膜」は実年齢より老けている? 写真1枚でAIが疾患リスクを推定
- 50万人の情報が流出した英国バイオバンクのインシデントでPETs利用は拡大するか
- がんの微小病変解析をより正確に、1台で核酸抽出から定量を自動処理する装置
- 猛暑の夏を乗り切る! 冷却性能20%増の首元デバイスで−2℃体験へ
コーナーリンク



