米国が強化を進める手術ロボットの安全対策:海外医療技術トレンド(5)(2/3 ページ)
手術ロボットの安全対策を強化するFDA
米国では、外科医から起業家に転身したフレドリック・モール博士が立ち上げた外科手術システムのダヴィンチで著名なIntuitive Surgical(インテュイティブサージカル)など、医師主導の医療技術ベンチャー企業(Med-Tech)が相次ぎロボット手術支援システムの開発に参入し、ベンチャーキャピタルやアクセラレーターによる起業サポート体制も整備されてきた。
また2015年3月、共同でロボット支援手術プラットフォームを開発することを発表したJohnson&Johnson(ジョンソン・エンド・ジョンソン)とGoogle(グーグル)など、異業種から手術ロボットの分野への参入を狙う企業も増えている。
このように手術ロボット市場が拡大し、競争が激化する中で、業界全体の共通課題になっているのが、市販後の医療安全対策だ。FDAは「MedWatch」という安全情報・有害事象報告システムを構築し(関連情報)、市販後安全対策の徹底を図ってきたが、RAS機器に関連する医療機器報告書(MDRs)の件数は年々増加している。
さらに、ロボット支援低侵襲外科手術の分野でリコール事案が相次いだり、手術ロボット使用に関する医師の習熟度やトレーニング体制に対する懸念が高まったりしたことを受けて、FDAが医療安全対策を強化する姿勢を打ち出した。
2015年7月、FDAは「ロボット支援手術(RAS)機器:課題と機会」と題する公開ワークショップを開催している(参考情報)。2日間のワークショップを通じて、以下のようなテーマが公開討議された。
- 新たなRAS機器プラットフォームの基本的な技術面およびパフォーマンス面の特徴は何か? 市販のRAS機器プラットフォームを繰り返し修正するために、基本的な技術面およびパフォーマンス面の特徴は何か?
- RAS機器プラットフォームおよびそれらとともに使用する他の医療機器の間の相互運用性をどのようにして評価すべきか? その場合、どのようなエビデンスを提供すべきか? 相互運用性を推進すべきか?
- RAS機器で「一般」用途の表示と「特定」の表示を区別する際に考慮する点は何か?
- 既にRAS機器が一般用途で承認されている場合、どのような環境下で、特定の手術手技の表示を補完するための追加データが必要となるか?
- 機器のユーザビリティを保証し、リスクを低減する際、市販前評価における訓練やシミュレーションの役割は何か?
- 複数目的のために効果的に活用できるデータソースを改善・構築するために、すべてのステークホルダー間でどのような協業を推進することが可能か?
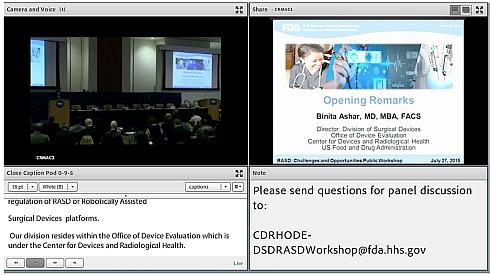 図2 FDA公開ワークショップ(2015年7月)の様子(クリックで拡大) 出典:FDA「Public Workshop - Robotically-Assisted Surgical Devices: Challenges and Opportunities」(2015年7月)
図2 FDA公開ワークショップ(2015年7月)の様子(クリックで拡大) 出典:FDA「Public Workshop - Robotically-Assisted Surgical Devices: Challenges and Opportunities」(2015年7月)他の医療機器や医薬品と比較して、歴史の浅い手術ロボットは、市販後の安全な使用や、維持メンテナンス、廃棄に至るまでのライフサイクル管理に関する経験/ノウハウが不足しており、監視する側も監視を受ける側も人材の層が薄いのが、米国の現状だ。
Copyright © ITmedia, Inc. All Rights Reserved.
医療機器の記事ランキング
- 脳動脈瘤の治療をより安全に テルモが細径対応の新デバイス発売
- 75秒で精子濃度など20項目を自動解析 男性不妊検査向け装置を提案
- 知人より見知らぬ他人とシンクロ? スポーツ観戦の熱狂を科学的に解明
- 約10秒で検温完了 ケースごと丸洗い可能なテルモの新型体温計
- 抗体薬などの体内動態を追跡、数週間の長期PET撮像を実現
- 生きた乳酸菌は代謝、死んだ乳酸菌は免疫へ 状態で異なる腸内効果
- 厚さ約25μmの神経シートを開発、光刺激と記録を同時に実現
- 日立ら肺がん細胞診の新解析技術 SEMと元素分析で検体評価を支援
- 50万人の情報が流出した英国バイオバンクのインシデントでPETs利用は拡大するか
- あなたの「網膜」は実年齢より老けている? 写真1枚でAIが疾患リスクを推定
コーナーリンク



