父親の低タンパク質の食事が子どもの代謝変化に影響するメカニズムを発見:医療技術ニュース
理化学研究所は、父親の低タンパク質の食事が生殖細胞でエピゲノム変化を誘導し、それが精子を通じて子どもに伝わることで、肝臓の遺伝子発現変化と代謝変化を誘導することを明らかにした。
理化学研究所は2020年3月20日、父親の低タンパク質の食事が生殖細胞でエピゲノム変化を誘導し、それが精子を通じて子どもに伝わることで、肝臓の遺伝子発現変化と代謝変化を誘導することを発見したと発表した。筑波大学、大阪大学、九州大学、東京大学、ストラスブール大学との国際共同研究グループによる成果となる。
今回の研究では、低タンパク質食またはコントロール食で飼育した野生型の雄マウスをコントロール食で飼育した野生型雌マウスと交配させ、その子どもの肝臓の遺伝子発現パターンを調べた。その結果、低タンパク質食の雄マウスの子どもは、コントロール食の雄マウスの子どもと比べて遺伝子発現の変化が見られた。発現上昇した遺伝子には、コレステロール代謝系遺伝子などが多く含まれていた。
一方、ATF7ヘテロ変異マウスの子どもでは、父親の低タンパク質食による遺伝子の発現変化はなかった。ATF7は、マウスなどにおいて、ストレスなど環境要因によるエピゲノム変化の誘導に重要な転写因子だ。
次に、低タンパク質食のATF7への影響を調べたところ、父親の精巣の生殖細胞ではATF7がリン酸化され、標的遺伝子から遊離することで、エピゲノム変化が起こっていることが明らかとなった。この変化は精子を経て受精卵に伝わり、子どもの遺伝子発現を変化させることが示された。
これらの研究成果から、「親の食事が子どもの疾患、特に糖尿病などの生活習慣病の発生頻度に影響する」という胎児プログラミング仮説のメカニズムの一端が解明されたことになる。今後、生活習慣病などの発症予防につながることが期待される。
- 知人より見知らぬ他人とシンクロ? スポーツ観戦の熱狂を科学的に解明
- 厚さ約25μmの神経シートを開発、光刺激と記録を同時に実現
- 生きた乳酸菌は代謝、死んだ乳酸菌は免疫へ 状態で異なる腸内効果
- あなたの「網膜」は実年齢より老けている? 写真1枚でAIが疾患リスクを推定
- 50万人の情報が流出した英国バイオバンクのインシデントでPETs利用は拡大するか
- ミカンの1種“タチバナ”にシミ抑制効果、メラニンの蓄積を阻害
- セラミド不足がアトピー性皮膚炎の直接原因であることを実証
- エッジAI搭載の前眼部検査機で白内障など早期発見へ、従来機より低コスト化も
- 外科医と対話する生成AI、胃がん手術の実証実験で有用性80%達成
- 医療機器大手ストライカーの事例に見る米国サイバーインシデント情報開示の複雑性
関連記事
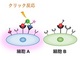 生体内のがん組織を指紋認証のように識別する標識化技術を開発
生体内のがん組織を指紋認証のように識別する標識化技術を開発
理化学研究所は、細胞上で人工糖ペプチドを合成することで、指紋認証のようにがん細胞をパターン認識し、そのパターンを利用してマウス体内で特定のがん組織を標識化することに成功した。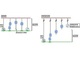 神経幹細胞が再形成する仕組みを発見
神経幹細胞が再形成する仕組みを発見
京都大学と理化学研究所の研究グループは、哺乳類の脳の形成段階において、神経幹細胞が形態を柔軟に再形成する仕組みを発見した。脳形成の基本的な仕組みが解明されたことで、脳形成不全に伴う疾患などの原因解明に役立つことが期待される。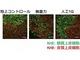 宇宙の無重力空間で委縮した胸腺は、人工重力で軽減することを解明
宇宙の無重力空間で委縮した胸腺は、人工重力で軽減することを解明
理化学研究所は、無重力空間を経験すると胸腺が委縮すること、その委縮は人工的な重力負荷で軽減すること、委縮が胸腺細胞の増殖抑制によって起こるという仕組みを発見した。 臓器内の全細胞を調べる高速イメージングと高速解析技術を開発
臓器内の全細胞を調べる高速イメージングと高速解析技術を開発
理化学研究所は、透明化した臓器内の全ての細胞を解析する「全細胞解析」を実用化し、これを用いて、マウス脳を構成する約1億個の細胞を解析することに成功した。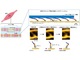 分子ナノシステムを設計し、筋収縮時の分子の動きを捉えることに成功
分子ナノシステムを設計し、筋収縮時の分子の動きを捉えることに成功
理化学研究所は、筋収縮の最小機能単位であるサルコメア構造の一部を人工的に設計し、筋収縮の瞬間におけるモーター分子の動態を直接的に捉えることに成功した。肥大型心筋症の要因となるミオシン変異体を分子レベルで詳細に診断可能になる。
関連リンク
Copyright © ITmedia, Inc. All Rights Reserved.
医療機器の記事ランキング
- 脳動脈瘤の治療をより安全に テルモが細径対応の新デバイス発売
- 約10秒で検温完了 ケースごと丸洗い可能なテルモの新型体温計
- 厚さ約25μmの神経シートを開発、光刺激と記録を同時に実現
- 知人より見知らぬ他人とシンクロ? スポーツ観戦の熱狂を科学的に解明
- 生きた乳酸菌は代謝、死んだ乳酸菌は免疫へ 状態で異なる腸内効果
- 日立ら肺がん細胞診の新解析技術 SEMと元素分析で検体評価を支援
- あなたの「網膜」は実年齢より老けている? 写真1枚でAIが疾患リスクを推定
- 50万人の情報が流出した英国バイオバンクのインシデントでPETs利用は拡大するか
- がんの微小病変解析をより正確に、1台で核酸抽出から定量を自動処理する装置
- 猛暑の夏を乗り切る! 冷却性能20%増の首元デバイスで−2℃体験へ
コーナーリンク
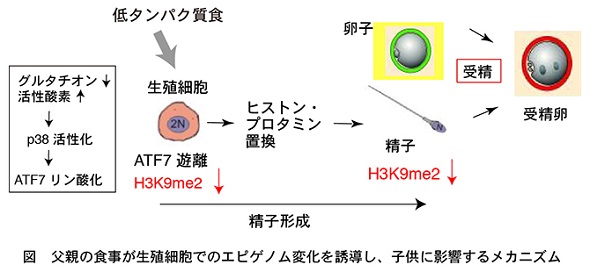
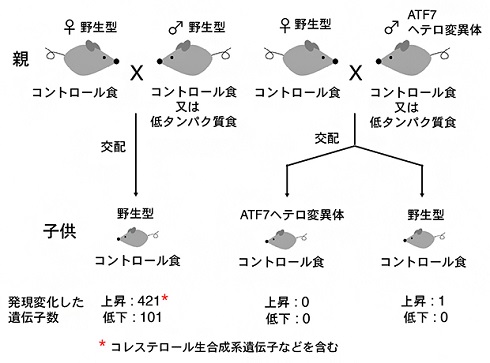 父親マウスの低タンパク質食による子どもマウスの肝臓での遺伝子発現変化 出典:理化学研究所
父親マウスの低タンパク質食による子どもマウスの肝臓での遺伝子発現変化 出典:理化学研究所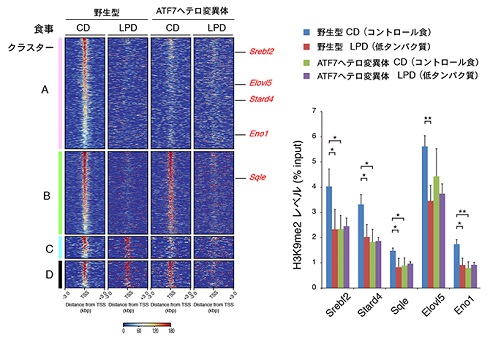
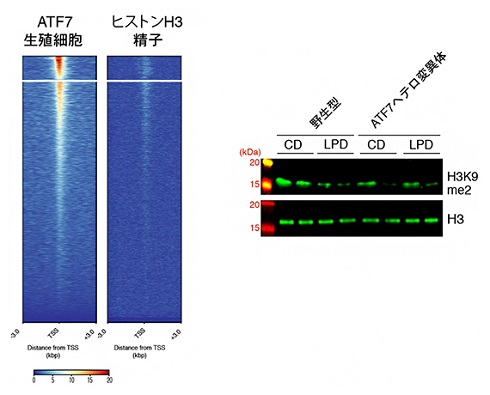 父親マウスの生殖細胞でのATF7結合遺伝子の解析 出典:理化学研究所
父親マウスの生殖細胞でのATF7結合遺伝子の解析 出典:理化学研究所


