がん手術の傷の炎症を抑える、内視鏡で噴霧可能な創傷被膜材を開発:医療機器ニュース
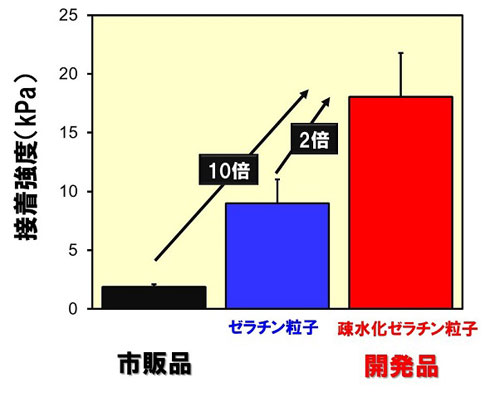
物質・材料研究機構と鹿児島大学は、消化管がん治療後の傷に内視鏡で噴霧できる創傷被膜材を開発した。市販被膜材の約10倍の接着力を有し、組織の修復とともに体内で分解するため、手術後の狭窄(きょうさく)などを予防する医療材としての応用が期待される。
物質・材料研究機構(NIMS)と鹿児島大学は2019年7月30日、消化管がん治療後の傷をふさぎ、組織の再生を促す、新しい創傷被膜材を開発したと発表した。
NIMSと鹿児島大学の共同研究グループは、組織接着性が高い疎水基を化学修飾した疎水化ゼラチンに、ブタ由来ゼラチンを合成して疎水化ゼラチン粒子を作成した。
この粒子は、マイクロメートルサイズの球状で、内視鏡用の噴霧装置で傷に吹き付けることで被覆材として使える。ブタ胃粘膜組織を用いた接着試験の結果では、市販の被膜材の約10倍、疎水化していないゼラチンの約2倍の接着強度を有していた。また、疎水化ゼラチン粒子同士が疎水性相互作用により凝集し、ゲルフィルム上の構造を形成することも分かった。
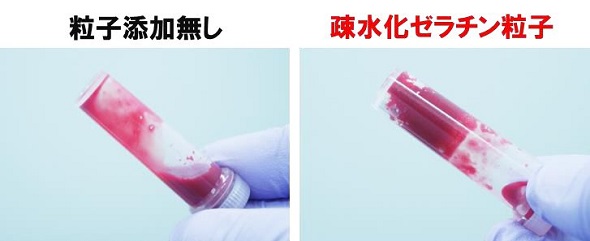
続いて、疎水化ゼラチン粒子をラット全血と混合したところ、血液凝固が認められた。さらに、ミニブタの胃に作製した人工潰瘍(かいよう)に同粒子を噴霧し、内視鏡的粘膜下層剥離術(ESD)のモデルとして治癒過程を観察した。その結果、粘膜下組織の炎症が軽減し、狭窄(きょうさく)の原因となる粘膜下層組織の線維化が抑制されていた。噴霧した疎水化ゼラチン粒子は生体組織の修復に伴い、体内で分解・吸収されるため、組織の修復後に再手術する必要はない。
ESDは早期消化管がんの低侵襲な治療法として注目を集めているが、露出した粘膜下層組織における炎症や狭窄が問題となっている。現在使用されているシート状の創傷被膜材は、組織接着性の低さや、分解に伴う炎症の発生、その形状故に内視鏡を使って創傷部へ届けることが難しい、などの課題があった。
今回開発した被膜材は、生体組織に強く接着して傷を保護できるため、ESD後の狭窄や出血などを予防する医療材料としての応用が期待される。研究グループは今後、同材料の前臨床試験を進めるとしている。
- 脳動脈瘤の治療をより安全に テルモが細径対応の新デバイス発売
- 約10秒で検温完了 ケースごと丸洗い可能なテルモの新型体温計
- 日立ら肺がん細胞診の新解析技術 SEMと元素分析で検体評価を支援
- 細胞治療の調製から充填をシステムで自動化、品質のばらつき軽減へ
- がんの微小病変解析をより正確に、1台で核酸抽出から定量を自動処理する装置
- キヤノンが医療ITをブランド統合、AI解析で新ソリューションの展開へ
- ポリエチレン9割で構成した医療用滅菌包材のサンプル提供開始
- 微小重力下での細胞解析に向け、生細胞観察装置がISSへ打ち上げ
- AIで微細デバイスを鮮明に、低被ばく低造影剤の新型X線透視装置
- 高画質と低被ばくを実現、新型フォトンカウンティングが国内販売
関連記事
 がんプレシジョン医療にAIを活用、治療率が6倍に
がんプレシジョン医療にAIを活用、治療率が6倍に
がん研究会、がん研究所、FRONTEOヘルスケアは、最先端のゲノム解析技術とAI(人工知能)を用いて「がんプレシジョン医療」を実現するシステムの開発に向けた共同研究を開始する。現在、一般的で明確ながん治療法が当てはまらないがん患者の治療率は5%程度だが、共同研究により治療率を6倍の30%まで高められる可能性がある。 東北大学病院が個別化医療をスタート、がん治療にゲノム/オミックス解析を活用
東北大学病院が個別化医療をスタート、がん治療にゲノム/オミックス解析を活用
東北大学病院は、個々の患者に合わせた最適な治療を提案する「個別化医療」を推進するプロジェクトを開始した。まずは「個別化医療センター」が中心となって、疾患バイオバンクを設立し、がんクリニカルシーケンス検査を始める。 大腸がん幹細胞を標的とした治療モデルの開発に成功
大腸がん幹細胞を標的とした治療モデルの開発に成功
慶應義塾大学は、大腸がんの増殖をつかさどる「がん幹細胞」の詳細な機能の解析と、がん幹細胞を標的とした治療モデルの開発に成功した。がんの新たな根源的治療法の開発につながることが期待される。 がんを見つけて破壊するナノ粒子を合成する新たな方法を開発
がんを見つけて破壊するナノ粒子を合成する新たな方法を開発
名古屋大学は、2種類の試薬をアンモニア水に溶解するだけで、がん細胞を物理的・科学的に殺傷する多機能ナノ粒子を作製する方法を開発した。ナノ粒子はがん細胞を光らせ、内包する抗がん剤を放出する。 血液や尿に含まれるがんの診断マーカーを簡単に検知する技術を開発
血液や尿に含まれるがんの診断マーカーを簡単に検知する技術を開発
神奈川県立産業技術総合研究所は、血液や尿から、がんの診断マーカーとなる特定のマイクロRNAを簡単に検知する技術を開発した。血液や尿を98℃で2分間加熱処理した後に反応液と混合し、検査チップに滴下してマイクロRNAの有無を診断できる。
関連リンク
Copyright © ITmedia, Inc. All Rights Reserved.
医療機器の記事ランキング
- 脳動脈瘤の治療をより安全に テルモが細径対応の新デバイス発売
- 約10秒で検温完了 ケースごと丸洗い可能なテルモの新型体温計
- 厚さ約25μmの神経シートを開発、光刺激と記録を同時に実現
- 知人より見知らぬ他人とシンクロ? スポーツ観戦の熱狂を科学的に解明
- 生きた乳酸菌は代謝、死んだ乳酸菌は免疫へ 状態で異なる腸内効果
- 日立ら肺がん細胞診の新解析技術 SEMと元素分析で検体評価を支援
- あなたの「網膜」は実年齢より老けている? 写真1枚でAIが疾患リスクを推定
- 50万人の情報が流出した英国バイオバンクのインシデントでPETs利用は拡大するか
- がんの微小病変解析をより正確に、1台で核酸抽出から定量を自動処理する装置
- 猛暑の夏を乗り切る! 冷却性能20%増の首元デバイスで−2℃体験へ
コーナーリンク