医薬品候補分子の生体内移動を可視化する手法を開発:医療技術ニュース
京都大学は、医学や生理学分野で用いる「ホルマリン組織固定」の原理を拡張し、マウス脳内の小分子の分布を可視化する「FixEL法」を開発した。医薬品の候補となる小分子の動きを固定し、生体内での移動とタンパク質への結合を画像化できる。
京都大学は2022年12月5日、医学や生理学分野で用いる「ホルマリン組織固定」の原理を拡張し、マウス脳内の小分子の分布を可視化する「FixEL法」を開発したと発表した。医薬品の候補となる小分子の動きを固定することで、小分子の生体内移動とタンパク質への結合を高い解像度で画像化できる。
治療薬や診断薬にはさまざまな小分子が用いられるが、体内で疾患に関係するタンパク質と結合することで、機能を発揮する。そのため医薬品の開発には、小分子が体内のどこへ移動し、どのタンパク質と結合するかなどを調べる必要がある。
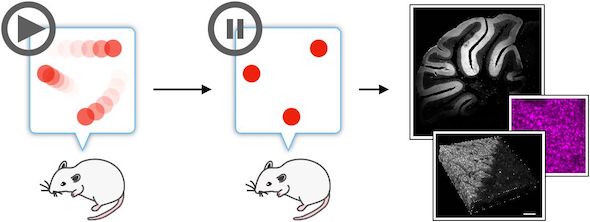
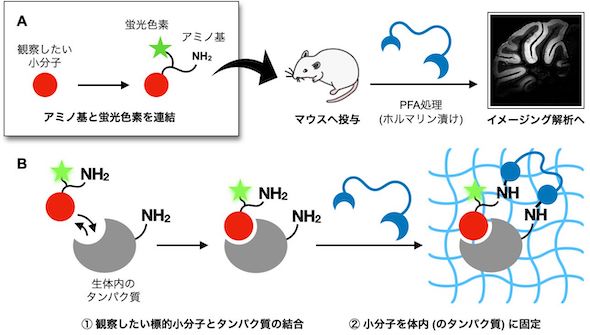
今回の研究では、ホルマリン漬けに使用するPFA(パラホルムアルデヒド)に着目。アミノ基と蛍光色素を連結させた小分子をマウスに投与後、PFAを全身に処理することで、組織の固定と同時に蛍光色素を固定し、その瞬間の小分子の体内位置をμmの解像度で可視化した。
実際に、FixEL法によって小分子の分布を画像化できるか調べるため、脳に存在するmGlu1(代謝型グルタミン受容体1)と結合する小分子のmGlu1リガンドを標的として実験した。共焦点レーザー顕微鏡を用いて、分子を固定した脳組織を観察したところ、mGlu1が豊富に存在する小脳分子層で蛍光が検出できた。
より高倍率で観察すると、粒状の蛍光シグナルが小脳分子層に集まっていることが分かった。このシグナルは、mGlu1の分布と一致することも確認した。これらのことから、生きたマウスの脳内で特定のタンパク質に標的小分子が結合しており、その様子をFixEL法で高解像度に解析できることが示された。
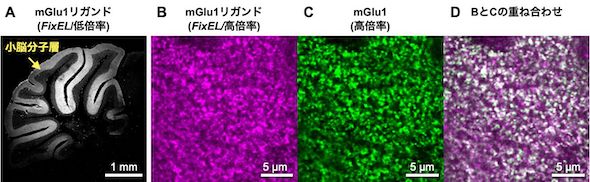 (A)mGlu1リガンドをFixEL法で固定したマウス小脳の蛍光観察画像。(B)小脳分子層を拡大した観察結果。(C)Bと同じ領域のmGlu1タンパク質分布。(D)BとCの画像の重ね合わせ。白いほど、よく分布が一致している[クリックで拡大] 出所:京都大学
(A)mGlu1リガンドをFixEL法で固定したマウス小脳の蛍光観察画像。(B)小脳分子層を拡大した観察結果。(C)Bと同じ領域のmGlu1タンパク質分布。(D)BとCの画像の重ね合わせ。白いほど、よく分布が一致している[クリックで拡大] 出所:京都大学FixEL法ではPFAを処理する瞬間に小分子の位置が固定されるため、複数のマウスに異なるタイミングでPFA処理し、標的小分子の体内移動を調査した。その結果、それぞれのマウスで異なる蛍光分布が見られ、mGlu1がどのように脳内を移動しているかを経時的に捉えることができた。
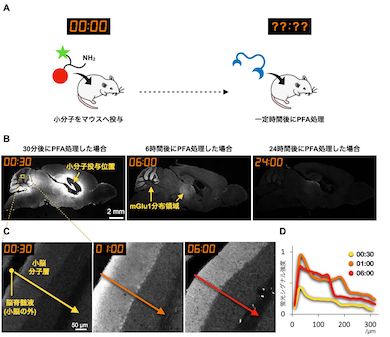 (A)小分子の体内分布の時間変化を調べる実験の手順。(B)mGlu1リガンドを投与したマウスの全脳スライス蛍光観察画像。投与からそれぞれ30分、6時間、24時間後にPFAで固定処理した。(C)小脳の一部を拡大した蛍光観察画像。mGlu1リガンドの投与から30分〜6時間後にPFA処理した。(D)Cの画像上の矢印上の蛍光シグナル強度をグラフ化したもの。30分や1時間の時点で、小脳分子層の中でも特に脳脊髄液に触れている領域の蛍光シグナル強度が高い。これはmGlu1リガンドが脳脊髄液側から小脳分子層へ浸透していることを反映している[クリックで拡大] 出所:京都大学
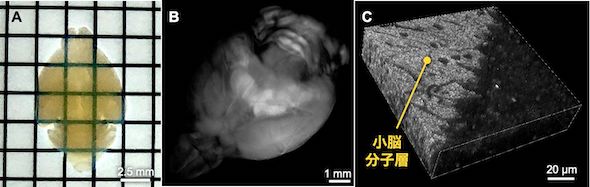
(A)小分子の体内分布の時間変化を調べる実験の手順。(B)mGlu1リガンドを投与したマウスの全脳スライス蛍光観察画像。投与からそれぞれ30分、6時間、24時間後にPFAで固定処理した。(C)小脳の一部を拡大した蛍光観察画像。mGlu1リガンドの投与から30分〜6時間後にPFA処理した。(D)Cの画像上の矢印上の蛍光シグナル強度をグラフ化したもの。30分や1時間の時点で、小脳分子層の中でも特に脳脊髄液に触れている領域の蛍光シグナル強度が高い。これはmGlu1リガンドが脳脊髄液側から小脳分子層へ浸透していることを反映している[クリックで拡大] 出所:京都大学また、mGlu1リガンド以外にも、医薬品として使用中の小分子や新タイプの医薬品として期待される小型抗体が同様の原理で画像化できることを確認。さらに、化学的に組織を透明化する技術により、組織を薄切りにすることなく、小分子の組織内での位置を3次元的に捉えることに成功した。
医薬品の候補となる分子の多くは、分子量が500以下の小分子だ。小分子の組織内での分布を詳細に解析することで、医薬品や診断薬の効率的な開発が期待される。
- 知人より見知らぬ他人とシンクロ? スポーツ観戦の熱狂を科学的に解明
- 厚さ約25μmの神経シートを開発、光刺激と記録を同時に実現
- 生きた乳酸菌は代謝、死んだ乳酸菌は免疫へ 状態で異なる腸内効果
- あなたの「網膜」は実年齢より老けている? 写真1枚でAIが疾患リスクを推定
- 50万人の情報が流出した英国バイオバンクのインシデントでPETs利用は拡大するか
- ミカンの1種“タチバナ”にシミ抑制効果、メラニンの蓄積を阻害
- セラミド不足がアトピー性皮膚炎の直接原因であることを実証
- エッジAI搭載の前眼部検査機で白内障など早期発見へ、従来機より低コスト化も
- 外科医と対話する生成AI、胃がん手術の実証実験で有用性80%達成
- 医療機器大手ストライカーの事例に見る米国サイバーインシデント情報開示の複雑性
関連記事
 直近1カ月間のひきこもり傾向を評価する質問票を開発
直近1カ月間のひきこもり傾向を評価する質問票を開発
九州大学らは、直近1カ月間のひきこもり傾向を簡便に把握できる自記式質問票「HQ-25M」を開発した。オンライン調査の結果、ひきこもり傾向が高いほどHQ-25Mスコアが高いことが示され、同質問票の予備的妥当性が確認された。 北欧諸国が主導するデジタルヘルスの多国間連携
北欧諸国が主導するデジタルヘルスの多国間連携
本連載第32回、第45回、第51回、第57回で取り上げた北欧諸国のデータ駆動型デジタルヘルス施策が、多国間連携に向けて進化している。 皮膚上や体内に埋め込んで使用できるセンサー用極薄伸縮性導体を開発
皮膚上や体内に埋め込んで使用できるセンサー用極薄伸縮性導体を開発
理化学研究所は、皮膚上や体内埋め込み型センサーへの応用が期待される、厚さ約1.3μmの伸縮可能な導体を開発した。皮膚や臓器への密着性も良好で、生体情報取得のためのセンサー用電極として使用できることを確認している。 BioHEAとレーザー金属AMを組み合わせて、生体骨のような新材料を開発
BioHEAとレーザー金属AMを組み合わせて、生体骨のような新材料を開発
大阪大学は、バイオハイエントロピー合金とレーザー金属3Dプリンティングを組み合わせることで、強度と加工性に優れ、低弾性、生体親和性を兼ね備えた、生体骨のような新材料を開発した。人工関節や骨固定デバイスなどに適用できる。 天井全体に無影灯の機能を持たせる天井照明型手術室を開発
天井全体に無影灯の機能を持たせる天井照明型手術室を開発
大林組と大阪大学は、無影灯を必要としない天井照明型手術室「オペルミ」を開発した。術野を明るく照らす72基の「自動シューティングライト」と、手術室全体に均一な光を落とす「導光板パネル照明」で構成され、手術室の環境改善に寄与する。 難治性前立腺がんのアルファ線治療に使用する放射性リガンドを開発
難治性前立腺がんのアルファ線治療に使用する放射性リガンドを開発
大阪大学は、前立腺がんのアルファ線治療を目的とした放射性リガンドを開発し、マウスを用いた実験で腫瘍の縮小効果が長期間持続することを確認した。難治性前立腺がんに対する医師主導治験の開始を準備している。
関連リンク
Copyright © ITmedia, Inc. All Rights Reserved.
医療機器の記事ランキング
- 脳動脈瘤の治療をより安全に テルモが細径対応の新デバイス発売
- 約10秒で検温完了 ケースごと丸洗い可能なテルモの新型体温計
- 厚さ約25μmの神経シートを開発、光刺激と記録を同時に実現
- 知人より見知らぬ他人とシンクロ? スポーツ観戦の熱狂を科学的に解明
- 生きた乳酸菌は代謝、死んだ乳酸菌は免疫へ 状態で異なる腸内効果
- 日立ら肺がん細胞診の新解析技術 SEMと元素分析で検体評価を支援
- あなたの「網膜」は実年齢より老けている? 写真1枚でAIが疾患リスクを推定
- 50万人の情報が流出した英国バイオバンクのインシデントでPETs利用は拡大するか
- がんの微小病変解析をより正確に、1台で核酸抽出から定量を自動処理する装置
- 猛暑の夏を乗り切る! 冷却性能20%増の首元デバイスで−2℃体験へ
コーナーリンク