「トラウマ」はなぜ覚えている? 嫌悪記憶を上書き保存する脳メカニズムを解明:医療技術ニュース
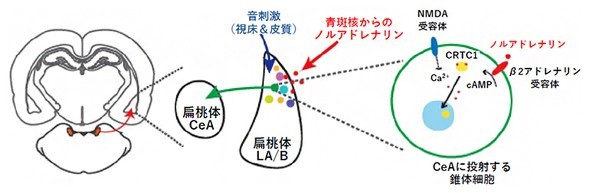
理化学研究所は、嫌悪記憶が想起される際に脳が記憶を再固定化する神経回路と分子機構を解明した。青斑核からノルアドレナリンが放出され、扁桃体におけるβ2アドレナリン受容体と転写因子を介して再固定化する。
理化学研究所は2026年3月4日、ラットを用いて、嫌悪記憶が想起された際に脳が記憶を再固定化する神経回路メカニズムと分子機構を明らかにしたと発表した。PTSD(心的外傷後ストレス障害)などで、恐怖などの嫌悪記憶が過度に強化される仕組みの理解が期待される。東京大学、沖縄科学技術大学院大学との共同研究による成果だ。
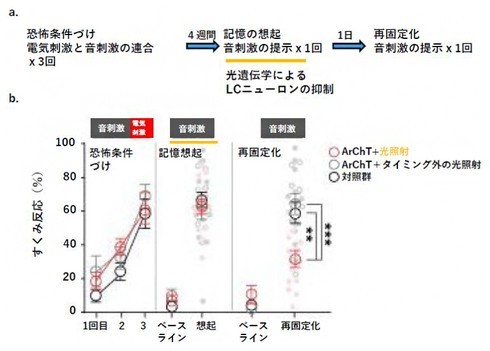
記憶は想起されるたびに一時的に不安定化し、最新情報に基づいて更新、再編され再固定化する。研究グループは、嫌悪記憶でのこのプロセスにおいて、脳幹の青斑核におけるノルアドレナリン作動性ニューロンの活動が中心的な役割を担うことを、光遺伝学法を用いた実験で特定した。
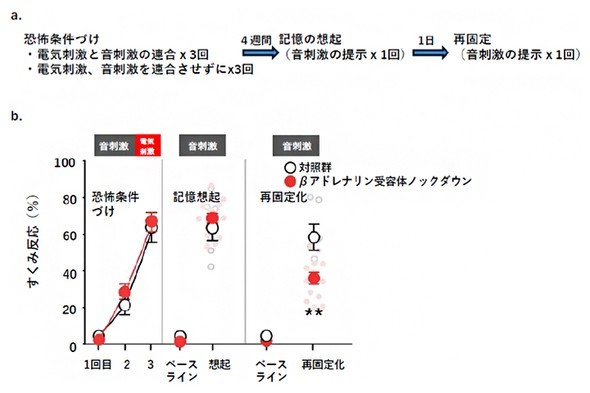
嫌悪記憶の想起に伴い青斑核から放出されたノルアドレナリンが、扁桃体の外側核および基底外側核(LA/B)から中央核(CeA)へ投射するニューロンに存在するβ2アドレナリン受容体を介して作用し、記憶を再固定化する。
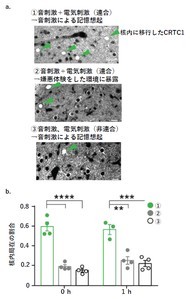
さらに分子レベルの解析により、ノルアドレナリンのシグナルが転写因子コアクチベーターCRTC1を細胞核内へ移行させ、再固定化に必要な遺伝子発現を誘導することを解明した。CRTC1をノックダウンして阻害すると再固定化のみが障害されることから、CRTC1が記憶の更新に不可欠であることが明らかになった。
実験では、記憶想起直前に軽度なストレスを与えることで再固定化が強化される現象も確認された。
同研究は、記憶の再固定化を制御する脳回路から受容体、核内シグナルに至る一連の仕組みを包括的に示した初めての成果だ。今後はβ2アドレナリン受容体やCRTC1経路を標的とした、PTSDや不安障害などの新規治療法および心理的介入アプローチの開発への展開が期待される。
関連記事
 頭の中の映像をテキストに変換する技術を開発
頭の中の映像をテキストに変換する技術を開発
NTTは、ヒトが見た映像や思い浮かべた情景の内容を脳活動から文章として生成する技術「マインド・キャプショニング」を開発した。非言語的思考を言語化する脳解読の新手法となる。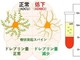 血液検査で認知症の予兆をキャッチする技術を開発
血液検査で認知症の予兆をキャッチする技術を開発
東京大学は、血液や髄液中のタンパク質ドレブリンを測定することで、アルツハイマー病による軽度認知障害を早期に診断できる技術を開発した。従来の病理指標とは異なる新しいタイプのバイオマーカーだ。 資生堂の新美容液を生み出す「fibona」とは、最小工場発のアジャイル型モノづくり
資生堂の新美容液を生み出す「fibona」とは、最小工場発のアジャイル型モノづくり
資生堂は共創プログラム「fibona」より新美容液を発表。独自技術で成分結晶化の課題を解決した。研究所併設の最小工場を活用し、プロトタイプを市場と共に磨き上げるアジャイルなモノづくり手法に迫る。 跳んでも走ってもノイズなく筋電図を計測する衣服型デバイスを開発
跳んでも走ってもノイズなく筋電図を計測する衣服型デバイスを開発
理化学研究所と東京大学は、動作中でも全身の筋電図を高精度に取得できる衣服型デバイスを開発した。ノイズを抑制する伸縮性同軸配線を採用し、医療やスポーツなど幅広い応用が期待される。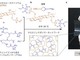 塩水中などの自然環境で速やかに分解する丈夫なプラスチックを開発
塩水中などの自然環境で速やかに分解する丈夫なプラスチックを開発
理化学研究所は、豊富な天然資源の木材成分セルロースの誘導体を使用し、塩水中などの自然環境で速やかに分解する、しなやかで丈夫なプラスチックを開発した。塩化コリンの添加量で力学特性を制御できる。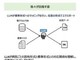 東大が医療特化型LLMを開発、医師国家試験の正答率93.3%
東大が医療特化型LLMを開発、医師国家試験の正答率93.3%
東京大学は、日本語医学知識を付与した医療特化型LLMを開発し、対話型AIサービスを公開した。医師国家試験ベンチマークの正答率は93.3%で、OpenAIの「GPT-4o」などの性能を上回った。
関連リンク
Copyright © ITmedia, Inc. All Rights Reserved.
医療機器の記事ランキング
- 生きた乳酸菌は代謝、死んだ乳酸菌は免疫へ 状態で異なる腸内効果
- 約10秒で検温完了 ケースごと丸洗い可能なテルモの新型体温計
- あなたの「網膜」は実年齢より老けている? 写真1枚でAIが疾患リスクを推定
- 日立ら肺がん細胞診の新解析技術 SEMと元素分析で検体評価を支援
- 猛暑の夏を乗り切る! 冷却性能20%増の首元デバイスで−2℃体験へ
- 50万人の情報が流出した英国バイオバンクのインシデントでPETs利用は拡大するか
- ミカンの1種“タチバナ”にシミ抑制効果、メラニンの蓄積を阻害
- 細胞治療の調製から充填をシステムで自動化、品質のばらつき軽減へ
- キヤノンが医療ITをブランド統合、AI解析で新ソリューションの展開へ
- がんの微小病変解析をより正確に、1台で核酸抽出から定量を自動処理する装置
コーナーリンク