不均一系触媒反応の機構と反応器:はじめての化学工学(12)(1/2 ページ)
前回は基本的な反応計算の考え方を解説しました。今回は固体触媒を用いた不均一系触媒反応を取り扱います。
触媒の役割とプロセス種別
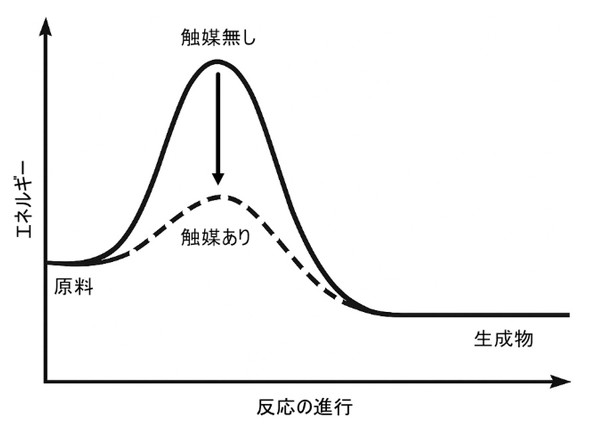
化学プラントで生産される製品の85%以上で触媒が使用されているといわれています。触媒は、それ自体は変化せずに化学反応の速度を向上させる物質です。反応に必要なエネルギーの山(活性化エネルギー)を低くする役割があります。
この触媒は、反応物との混ざり合い方によって「均一系」と「不均一系」に大別されます。
均一系触媒は反応物と同じ液体などに溶けて反応します。活性/選択性が高いですが、反応後に生成物と触媒を分離/回収するのが困難です。
対して不均一系触媒は、主に固体であり、気体や液体の反応物とは異なる相に存在します。反応後はろ過などにより触媒を分離できるため、回収/再利用が均一系触媒に比べて後処理が容易です。プロセス全体の生産性を考慮すると、実際の化学プラントでは不均一系触媒が基本的に選択されます。
触媒反応の7ステップ
不均一系触媒反応は、均一系触媒反応と比べて複雑なプロセスで進行します。流体が固体に接して流れるとき、その固体の表面には流れがほとんどない境膜(きょうまく)という層が存在します。この流れのない境膜の中を、原料が触媒の表面までたどり着くために原料が「拡散」して進みます。
気体の原料A固体触媒の表面で反応して気体の生成物になる「気固触媒反応」を例に挙げます。このプロセスは、7つのステップに分解できます。
- 外部拡散(境膜拡散):外側にある原料が、境膜を通って触媒表面へ移動する
- 内部拡散(細孔内拡散):原料が触媒の細孔を通り内部の活性点へ移動する
- 吸着:原料Aが活性点の表面に吸着する
- 表面反応:吸着した原料が活性点上で反応し、生成物が得られる
- 脱離:生成物が活性点から離れる
- 内部拡散(細孔内拡散):生成物が細孔を通り触媒の外部表面へ移動する
- 外部拡散(境膜拡散):生成物が触媒表面から離れて外部へ出ていく
これら7つのステップはつながっています。プロセス全体の速度は、この中で最も遅いステップによって支配されます。この最も遅いステップを「律速段階」と呼びます。律速段階がどのステップになるかによって、反応の挙動は大きく反応律速と拡散律速の2つに分類されます。
表面での化学反応(ステップ3〜5)が最も遅い場合は反応律速になります。このとき、全体の反応速度は触媒固有の化学的な性能に依存します。反応律速は、触媒のポテンシャルを最大限に引き出せていることを意味します。
対して、原料や生成物の物理的な移動(ステップ1、2、6、7)が最も遅い場合は拡散律速になります。どんなに高性能な触媒を使っても、原料が活性点にたどり着けなかったり、生成物が活性点から離れられなかったりするため、触媒の能力が十分に発揮されません。
Copyright © ITmedia, Inc. All Rights Reserved.
コーナーリンク