未知の反応を予測できる機械学習 スーパーハイドライドの合成過程を解明:研究開発の最前線
東京大学は、スーパーハイドライドと呼ばれる超高密度水素化物の合成過程を理論的に解明した。第一原理計算を模倣する機械学習ポテンシャルを構築し、分子動力学シミュレーションによって原子レベルで解析した。
東京大学は2025年6月5日、「スーパーハイドライド」と呼ばれる超高密度水素化物の合成過程を理論的に解明したと発表した。東北大学とケンブリッジ大学との共同研究で、第一原理計算を模倣するML(機械学習)ポテンシャルを構築し、分子動力学シミュレーションによって原子レベルで解析した。
水素含有量が非常に高いスーパーハイドライドは、水素貯蔵材料として注目されている。しかし、合成には数十ギガパスカル(GPa)の高圧が必要で反応の制御が難しく、高圧下における熱分析などの手法が限られていることが、反応メカニズムの分析の妨げとなっていた。
研究グループは、水素の含有量が異なるデータや高温での不安定な構造をあらかじめデータとして取り込み、反応過程に出現し得る不安定な構造を含めて学習したMLモデルを構築。未知の反応経路にも対応し、暗黙的に反応中の構造を再現できるようになった。
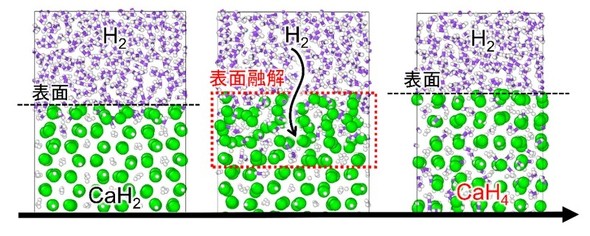
このMLモデルを用いた分子動力学シミュレーションで、カルシウム水素化物(CaH2)がカルシウムスーパーハイドライド(CaH4)に変化する過程を再現したところ、高温、高圧環境下ではCaH2の表面が一時的に液状化することが分かった。液体状態では水素の動きは速く、水素を効率的に取り込める。水素化反応が終了すると、安定なCaH4の固相が形成された。
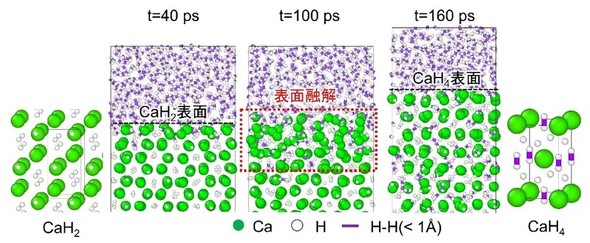 高温、高圧(1200℃、40GPa)でのCaH4合成反応の分子動力学シミュレーション。材料表面が溶けて乱れ、水素分子(紫線、大きさは1オングストローム、100億分の1m以下)が吸収されていく。反応が完全に進行すると分子状の水素のようなものを含んだCaH4の固相が得られる。シミュレーションの時間スケール(t)は、ピコ秒(1兆分の1秒)[クリックで拡大] 出所:東京大学
高温、高圧(1200℃、40GPa)でのCaH4合成反応の分子動力学シミュレーション。材料表面が溶けて乱れ、水素分子(紫線、大きさは1オングストローム、100億分の1m以下)が吸収されていく。反応が完全に進行すると分子状の水素のようなものを含んだCaH4の固相が得られる。シミュレーションの時間スケール(t)は、ピコ秒(1兆分の1秒)[クリックで拡大] 出所:東京大学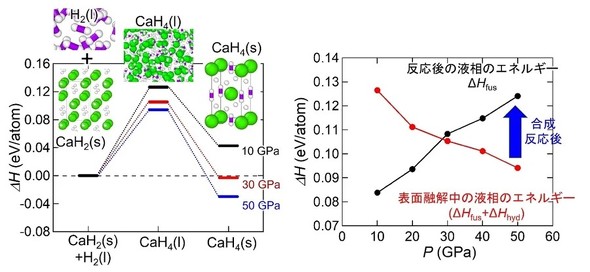 CaH4の合成反応中の各状態のエネルギーの圧力依存性。(左)圧力を上げると固相(s)と液相(l)のCaH4両方が安定化して縦軸のエネルギーの値が下がり、表面の液化を介した反応が起こりやすくなる。(右)水素化反応が終了すると水素化のエネルギー分、液相CaH4が不安定になり固体に戻る[クリックで拡大] 出所:東京大学
CaH4の合成反応中の各状態のエネルギーの圧力依存性。(左)圧力を上げると固相(s)と液相(l)のCaH4両方が安定化して縦軸のエネルギーの値が下がり、表面の液化を介した反応が起こりやすくなる。(右)水素化反応が終了すると水素化のエネルギー分、液相CaH4が不安定になり固体に戻る[クリックで拡大] 出所:東京大学今後、圧力と水素化反応によって引き起こされる反応メカニズムの解明により、スーパーハイドライドの実用化に向けた、精密制御が期待される。また、水素貯蔵材料の未知反応の予測と再現を可能としたMLモデルは、合成可能性の探索に寄与する。
関連記事
 偶然の出会いから紫綬褒章へ、東大の岡部教授が語るチタン製錬への思い
偶然の出会いから紫綬褒章へ、東大の岡部教授が語るチタン製錬への思い
令和5年春の紫綬褒章受章が決定した東京大学 生産技術研究所 教授 岡部徹氏に、紫綬褒章受章への思いやレアメタルの研究を開始した経緯、現在注力している研究、今後の展開について聞いた。 高効率で実用的な光触媒反応システムを開発 水素と酸素の発生セルを独立
高効率で実用的な光触媒反応システムを開発 水素と酸素の発生セルを独立
名古屋大学らは高効率かつ実用的な水分解光触媒反応システムを開発した。 リチウムイオン電池リサイクル技術の現在地
リチウムイオン電池リサイクル技術の現在地
本連載では東北大学大学院 工学研究科附属 超臨界溶媒工学研究センターに属する研究グループが開発を進める「リチウムイオン電池リサイクル技術の水熱有機酸浸出プロセス」を紹介する。最終回となる第6回ではこれまでのまとめとリチウムイオン電池に関する研究論文の特徴を取り上げる。 半導体製造フォトリソグラフィ工程で使用する高純度現像液を再生する新工場
半導体製造フォトリソグラフィ工程で使用する高純度現像液を再生する新工場
長瀬産業、ナガセケムテックス、Sachemの合弁会社であるSN Techが、半導体製造に使用する高純度現像液TMAHを回収、再生する新工場「SN Tech 東大阪第二工場」を開設した。 東大物性研が研究機関向けヘリウムリサイクル事業を開始、将来的には企業向けも
東大物性研が研究機関向けヘリウムリサイクル事業を開始、将来的には企業向けも
2019年10月1日から、東京大学物性研究所(東大物性研)がヘリウムガスの再液化事業をスタートする。研究用途だけでなく産業用途でも広く利用されているヘリウムは供給不足に陥りつつあるが、それをリサイクルによってカバーしたい狙いがある。
関連リンク
Copyright © ITmedia, Inc. All Rights Reserved.
コーナーリンク