細菌の薬剤耐性化の原因となる因子とその発現メカニズムを解明:医療技術ニュース
筑波大学と京都産業大学らは、抗菌薬への耐性に関係するタンパク質ARE-ABCFの遺伝子を、院内感染の原因となるディフィシル菌で発見し、その機能を明らかにした。
筑波大学と京都産業大学は2023年3月27日、抗菌薬への耐性に関係するタンパク質ARE-ABCF(antibiotic resistance ATP-binding cassette-F protein subfamily)の遺伝子をディフィシル菌で発見し、その機能を明らかにしたと発表した。
ディフィシル菌は、抗菌薬の使用などにより、増殖すると常在腸内細菌叢の乱れを引き起こし、下痢などを症状とするディフィシル感染症の原因となる。一方、ARE-ABCF遺伝子は、ディフィシル菌を含むクロストリジア綱の細菌の染色体に幅広く保存されていた。
研究グループは、ディフィシル菌のARE-ABCF遺伝子が、リンコサミド系とプレウロムチリン系の抗菌薬に対する薬剤耐性を媒介することを明らかにし、同遺伝子をcpIR(Clostridial pleuromutilin and lincosamide resistance)と命名した。
また、ディフィシル菌が、cpIRと可動性因子にコードされている薬剤耐性遺伝子ermBを同時に持つことで、リンコサミド系抗菌薬に対する耐性が相乗的に上昇することを見出した。
さらに、ディフィシル菌のcpIR発現が抗菌薬に応答して誘導されるメカニズムが明らかになった。cpIR mRNA上には、タンパク質CpIRをコードする領域以外にuORFと呼ばれるペプチドをコードする領域が存在する。抗菌薬がある場合は、リボソームと結合してuORFの翻訳が停止し、cpIR mRNAの二次構造が変化する。その結果、転写が終結せずに、転写の伸長と翻訳が促進される。
多くの細菌が有するARE-ABCFは院内感染の原因として知られているが、生物ごとに遺伝子配列が異なり、多様性や薬剤耐性との関係は解明されていなかった。また、ディフィシル感染症は、特にリンコサミド系抗菌薬の投与により発生することが示されており、ARE-ABCFとその遺伝子発現制御機構を標的とした予防、治療薬への応用が期待される。
- 知人より見知らぬ他人とシンクロ? スポーツ観戦の熱狂を科学的に解明
- 厚さ約25μmの神経シートを開発、光刺激と記録を同時に実現
- 生きた乳酸菌は代謝、死んだ乳酸菌は免疫へ 状態で異なる腸内効果
- あなたの「網膜」は実年齢より老けている? 写真1枚でAIが疾患リスクを推定
- 50万人の情報が流出した英国バイオバンクのインシデントでPETs利用は拡大するか
- ミカンの1種“タチバナ”にシミ抑制効果、メラニンの蓄積を阻害
- セラミド不足がアトピー性皮膚炎の直接原因であることを実証
- エッジAI搭載の前眼部検査機で白内障など早期発見へ、従来機より低コスト化も
- 外科医と対話する生成AI、胃がん手術の実証実験で有用性80%達成
- 医療機器大手ストライカーの事例に見る米国サイバーインシデント情報開示の複雑性
関連記事
 機能安全の基礎「機械安全規格」とは何か
機能安全の基礎「機械安全規格」とは何か
さまざまな産業機器の開発で必要不可欠な機能安全について「これだけは知っておきたいこと」を紹介する本連載。第1回は、機能安全の基礎となる「機械安全規格」を取り上げる。 医総会博覧会では内視鏡とカテーテルの手術を体験できる?
医総会博覧会では内視鏡とカテーテルの手術を体験できる?
オリンパスとテルモは「日本医学会総会2023東京 博覧会」に出展。内視鏡やカテーテルの体験コーナーを中心に一般来場者向けの展示を展開している。 生体器官の運動を再現できる、光駆動型オンチップ運動素子を作製
生体器官の運動を再現できる、光駆動型オンチップ運動素子を作製
日本電信電話は、生体器官の動きを再現できる、光駆動型オンチップ運動素子の作製に成功した。光刺激の制御により、腸管の分節運動と蠕動運動を生体器官に匹敵する性能で再現できた。 「世界初」軟質樹脂によるメタマテリアル3Dプリント技術、多分野での製品実装へ
「世界初」軟質樹脂によるメタマテリアル3Dプリント技術、多分野での製品実装へ
キョーラクは軟質樹脂による3Dプリント成形品の量産技術の確立に「世界で初めて」(同社)成功。同技術の製品実装の第1弾として、乳房を手術した人向けのインナーパッドをワコールと共同開発した。 20GHz超の周波数に対応した、世界最大規模の生体組織の電気定数データベース
20GHz超の周波数に対応した、世界最大規模の生体組織の電気定数データベース
情報通信研究機構は、1M〜100GHzの電波に対する、58種類の「生体組織の電気定数データベース」を公開した。周波数に応じた比誘電率、誘電損、電気伝導率のリストをwebサイト上で閲覧、ダウンロードできる。 Bluetoothを活用した次世代の聴覚補助技術と補聴器市場への影響を発表
Bluetoothを活用した次世代の聴覚補助技術と補聴器市場への影響を発表
Bluetooth SIGは、Bluetoothの新しいオーディオ規格「LE Audio」とBluetoothの新機能「Auracast ブロードキャスト オーディオ」が補聴器市場にもたらす影響などについて発表した。
関連リンク
Copyright © ITmedia, Inc. All Rights Reserved.
医療機器の記事ランキング
- 脳動脈瘤の治療をより安全に テルモが細径対応の新デバイス発売
- 厚さ約25μmの神経シートを開発、光刺激と記録を同時に実現
- 約10秒で検温完了 ケースごと丸洗い可能なテルモの新型体温計
- 知人より見知らぬ他人とシンクロ? スポーツ観戦の熱狂を科学的に解明
- 生きた乳酸菌は代謝、死んだ乳酸菌は免疫へ 状態で異なる腸内効果
- 日立ら肺がん細胞診の新解析技術 SEMと元素分析で検体評価を支援
- 50万人の情報が流出した英国バイオバンクのインシデントでPETs利用は拡大するか
- 75秒で精子濃度など20項目を自動解析 男性不妊検査向け装置を提案
- あなたの「網膜」は実年齢より老けている? 写真1枚でAIが疾患リスクを推定
- がんの微小病変解析をより正確に、1台で核酸抽出から定量を自動処理する装置
コーナーリンク
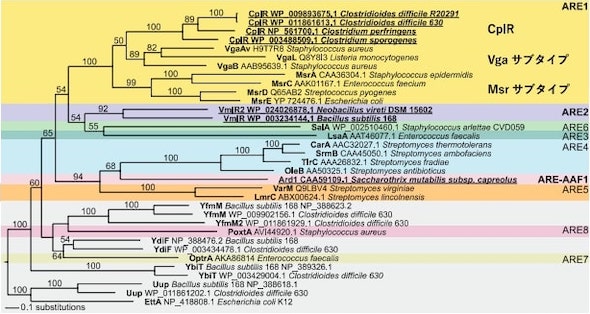 CplR、Ard1、VmlR2の遺伝子系統解析 出所:筑波大学
CplR、Ard1、VmlR2の遺伝子系統解析 出所:筑波大学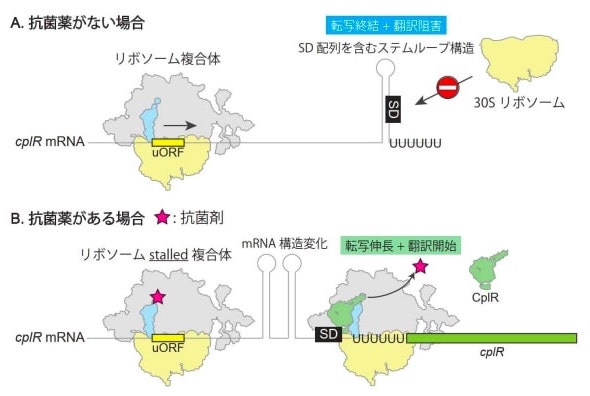 抗菌薬に応答したcpIR遺伝子発現機構のモデル 出所:筑波大学
抗菌薬に応答したcpIR遺伝子発現機構のモデル 出所:筑波大学


