そもそも鉄ってどんな金属?:鉄鋼材料の基礎知識(2)(2/3 ページ)
鉄の導電性
材料中の電気の通りやすさを示す指標である電気伝導率を見ると、鉄は11.2×106S/mです。アルミニウムは40×106S/mであり、鉄の約4倍の電気伝導率があります。銅は64.5×106S/mであり、鉄の約6倍の電気伝導率があります。(いずれも0℃のとき)[参考文献4]。つまり、鉄は比較的電気を通しにくい金属となります。そのため、鉄は電線や電子部品などの材料には適していません。
鉄の磁性
磁性とは、材料が磁場に置かれたときに反応する性質のことです。鉄が磁石とくっつくことは一般的に知られている話ですが、これは鉄が強い磁性をもっているためです。磁場を取り去った後も強い磁性を示すため、鉄は「強磁性体」と呼ばれています。鉄以外の金属では、コバルトとニッケルも強磁性体です。アルミニウムと銅は、あまり磁性をもたない「非磁性体」です。
ただし、鉄は常に磁性をもっているわけではありません。鉄は770℃以上になると、磁性を失います。材料が磁性を失う温度のことを「キュリー温度」または「キュリー点」といいます。
鉄の酸化特性
「鉄はサビやすい」というイメージをお持ちではないでしょうか。サビは金属の酸化反応が関与しており、金属が大気中の水や酸素と反応してイオン化することで生じます。各金属の酸化のしやすさは、「イオン化傾向」によって知ることができます。
図4に、金属をイオン化傾向が大きい順に並べています。イオン化傾向が大きい金属ほど、酸化しやすい金属となります。これを見ると、鉄は銅よりもイオン化傾向が大きく、アルミニウムよりもイオン化傾向が小さいことが分かります。つまり、鉄は銅よりも酸化しやすく、アルミニウムよりは酸化しづらい金属となります。
ただし、アルミニウムは一度酸化すると表面に薄い保護膜のようなものを形成するため、大気中ではそれ以上酸化が進みません。このような保護膜のことを「不動態皮膜(ふどうたいひまく)」といいます。鉄は不動態皮膜を形成しないため、大気中では一方的に酸化が進みます。鉄が激しくサビていることが多いのは、そのためです。ただし、鉄系材料の中にも「ステンレス鋼(こう)」のように不動態皮膜を形成するものがあります。
鉄の結晶構造
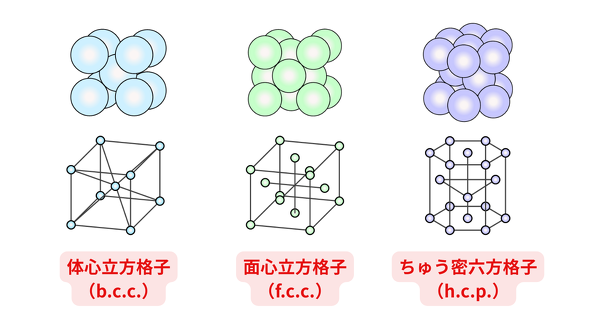
金属の性質は、その金属の結晶構造が大きく関係しています。結晶構造とは、原子が規則正しく配列した構造のことです。その構造の最小単位を「結晶格子」と呼びますが、結晶格子は原子の配置の仕方によって大きく「体心立方格子(body centered cubic lattice:bcc)」「面心立方格子(face centered cubic lattice:fcc)」「ちゅう密六方格子(hexagonal closed package lattice:hcp)」の3つの形があります。金属は、いずれかの結晶格子が無数に積み重なり、1つの固体を成しています。
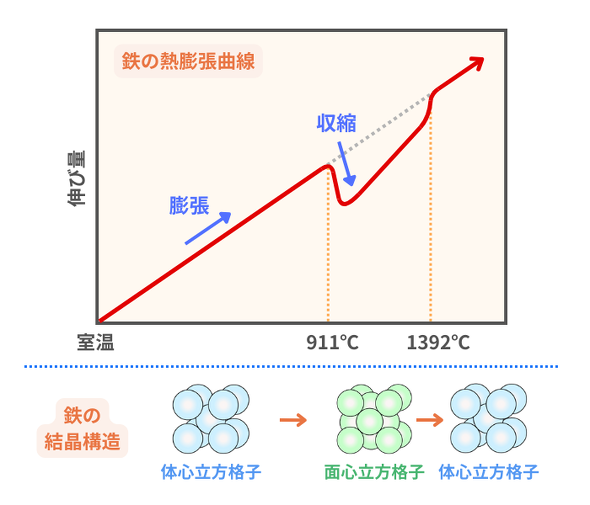
では、鉄の結晶構造はどうなっているのでしょうか。鉄は、温度によって結晶構造が異なります。室温から911℃までの温度域では、体心立方格子の形をとります。このときの鉄を「α(アルファ)鉄」といいます。911℃から1392℃までの温度域では、面心立方格子の形をとります。このときの鉄を「γ(ガンマ)鉄」といいます。1392℃から1535℃(融点)までの温度域では、再び体心立方格子の形をとります。このときの鉄を「δ(デルタ)鉄」といいます。つまり、鉄の結晶構造は室温では体心立方格子ですが、加熱していくと面心立方格子に変化し、さらに加熱を続けると体心立方格子に戻ります。
このように、鉄は温度によって2回結晶構造が変化する金属です。固体を維持しながら結晶構造が変わる現象のことを「同素(どうそ)変態」または「相(そう)変態」といいます。どの金属も同素変態するわけではなく、アルミニウムは同素変態しません。チタンやコバルトは同素変態しますが、変態の回数は1回だけです。鉄のように2回も同素変態する金属は珍しく、この現象が鉄に多様な特性をもたらしています。
加熱中に鉄が収縮する理由
先に説明したように、鉄は温度が上昇すると膨張し、長さと体積が増加します。ところが、911℃に達すると急激な収縮を起こします。これは、同素変態によって生じる原子充填率の減少が関係しています。
原子充填率とは、格子内に占める原子の割合のことです。鉄が室温でとる体心立方格子は、格子内の68%を原子が占めています。一方、鉄が911℃以上でとる面心立方格子は、格子内の74%を原子が占めています。後者の方が、原子が密な状態にあります。つまり、同素変態によって体心立方格子が面心立方格子に変化すると、原子がギュッと集まる方向に動きます。そのため、鉄が収縮を起こすのです。
Copyright © ITmedia, Inc. All Rights Reserved.
素材/化学の記事ランキング
コーナーリンク