シンガポールに学ぶクラウド型SaMD/Non-SaMDのセキュリティ:海外医療技術トレンド(117)(4/4 ページ)
IoTから医療機器に拡張されたサイバーセキュリティラベリング制度
本連載第101回および第106回で触れたように、シンガポール政府は、2020年10月、Non-SaMDを含む消費者向けIoT(モノのインターネット)製品を対象とするサイバーセキュリティラベリングスキーム(CLS(IoT)、関連情報)を世界に先駆けて導入している。
その後EUでは2024年12月10日、IoT製品のCEマーク表示を義務付けるサイバーレジリエンス法が発効し、2027年12月11日に主要規定が適用開始となる予定である(関連情報)。また米国では2025年1月7日、連邦通信委員会(FCC)が所管する消費者IoT製品向け認証/ラベリングプログラム「U.S.サイバートラストマーク」が正式にスタートしている(関連情報)。日本では、スマートホーム、工場、ビルなど、特定分野システムの製品を対象とする「セキュリティ要件適合評価及びラベリング制度(JC-STAR)」が、2025年3月から運用を開始する予定である(関連情報)。
他方、医療機器の領域では2024年10月16日、シンガポールサイバーセキュリティ庁(CSA)が、保健省(MOH)、保健科学庁(HSA)、Synapxe(旧IHiS)と協力して準備してきた「医療機器向けサイバーセキュリティラベリングスキーム(CLS(MD))」が、正式に導入された(関連情報)。このスキームは、CLS(IoT)の枠組みを医療機器に適用したものであり、2007年医療製品法(関連情報)や、本連載第69回で取り上げた国際医療機器規制当局フォーラム(IMDRF)の「医療機器サイバーセキュリティの原則および実践」(関連情報)に準拠しながら、アジア太平洋医療技術協会(APACMed、関連情報)やシンガポール製造業協会医療技術産業グループ(SMF - MTIG、関連情報)からの意見を参考にして策定された。
AIモデルまで踏み込んだシンガポールのSaMD規制ガイドライン
参考までに、SaMDのサイバーセキュリティについては、HSAが2024年3月1日に公表した「ソフトウェア医療機器に関する規制ガイドライン改訂第3版 - ライフサイクルアプローチ」(関連情報、PDF)の中で、以下のような点に関する考慮事項を提示している。
- セキュアな機器設計
- 顧客のセキュリティの文書化
- サイバーリスクマネジメント
- 検証と妥当性確認
- 継続的な調査計画と新たな脅威の迅速な検知
上記のうち、顧客のセキュリティの文書化では、本連載第82回で触れたソフトウェア部品表(SBOM)の有効活用について言及している。
加えてこのガイドラインでは、AI(人工知能)ベースのSaMDに関する規制についても触れている。図4は、ソフトウェア医療機器のAIモデルの具体例を示したものである。
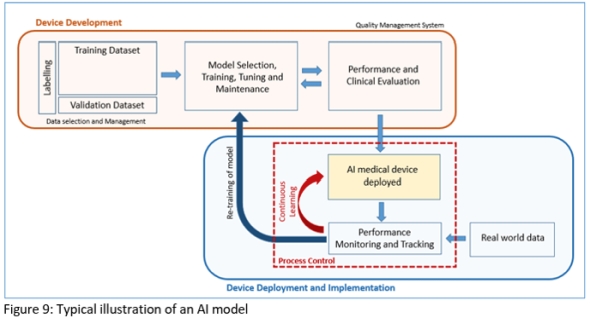 図4 ソフトウェア医療機器のAIモデルの例 出所:Health Sciences Authority「GL-04-R3 Regulatory Guidelines for Software Medical Devices - A Life Cycle Approach」(2024年3月1日)
図4 ソフトウェア医療機器のAIモデルの例 出所:Health Sciences Authority「GL-04-R3 Regulatory Guidelines for Software Medical Devices - A Life Cycle Approach」(2024年3月1日)そして、以下のような点について言及している。
- AI-MD向けの規制要求事項
- 継続的学習機能を有するAI-MD向けの追加的考慮事項
- AI-MDの市販後監視
- 登録済AI-MDに対する変更
シンガポールには、グローバル医療機器企業のアジア拠点が集中しており、シンガポール政府当局も、海外の医療機器サイバーセキュリティ規制への迅速な対応を進めている。加えて、クラウドコンピューティングの領域では、2025年2月12日、アマゾンがシンガポール事務所をAWSアジア太平洋ハブとして拡張することを発表するなど(関連情報)、AIをにらんだICT基盤の強化策が進んでおり、海外メドテックスタートアップ企業の誘致にも積極的だ。
筆者プロフィール
笹原英司(ささはら えいじ)(NPO法人ヘルスケアクラウド研究会・理事)
宮崎県出身。千葉大学大学院医学薬学府博士課程修了(医薬学博士)。デジタルマーケティング全般(B2B/B2C)および健康医療/介護福祉/ライフサイエンス業界のガバナンス/リスク/コンプライアンス関連調査研究/コンサルティング実績を有し、クラウドセキュリティアライアンス、在日米国商工会議所、グロバルヘルスイニシャチブ(GHI)等でビッグデータのセキュリティに関する啓発活動を行っている。
Twitter:https://twitter.com/esasahara
LinkedIn:https://www.linkedin.com/in/esasahara
Facebook:https://www.facebook.com/esasahara
関連記事
- ≫連載「海外医療技術トレンド」バックナンバー
 医療/介護イノベーションの“砂場”に変貌するシンガポール
医療/介護イノベーションの“砂場”に変貌するシンガポール
地域医療/介護連携ネットワークの共通基盤化が進み、主要プラットフォーム事業者のクラウドセンターが集中するシンガポール。今や、次世代健康/ウェルビーイング領域のイノベーションのためのテクノロジーサンドボックスに変貌している。 医療機器よりも難題!? Non-SaMDに影響が及ぶ米国のIoTセキュリティ政策
医療機器よりも難題!? Non-SaMDに影響が及ぶ米国のIoTセキュリティ政策
米国では、本連載第98回で取り上げた消費者IoT製品向け認証/ラベリングプログラム「U.S.サイバートラストマーク」の導入準備など、非医療機器/Non-SaMD(Software as a Medical Device)を取り巻く動きが加速している。 ソフトウェア部品表「SBOM」に着目、米国FDAの医療機器市販前セキュリティ対策
ソフトウェア部品表「SBOM」に着目、米国FDAの医療機器市販前セキュリティ対策
本連載第80回で、米国食品医薬品局(FDA)の2022会計年度医療機器ガイドライン策定計画を取り上げたが、早速、市販前サイバーセキュリティ要求事項に関する草案が公開された。 加速するEU医療機器規則とIMDRFセキュリティ原則の国際調和
加速するEU医療機器規則とIMDRFセキュリティ原則の国際調和
本連載第50回で、欧州の医療機器規制改革とサイバーセキュリティ動向を取り上げたが、新規則施行に向けた動きが本格化してきた。 正式発効する欧州保健データスペース「EHDS」で医療機器メーカーが果たす役割
正式発効する欧州保健データスペース「EHDS」で医療機器メーカーが果たす役割
本連載第70回から欧州連合(EU)の欧州保健データスペース(EHDS)構想を取り上げてきたが、ようやく正式に発効することが決まった。
Copyright © ITmedia, Inc. All Rights Reserved.
医療機器の記事ランキング
- 生きた乳酸菌は代謝、死んだ乳酸菌は免疫へ 状態で異なる腸内効果
- あなたの「網膜」は実年齢より老けている? 写真1枚でAIが疾患リスクを推定
- 日立ら肺がん細胞診の新解析技術 SEMと元素分析で検体評価を支援
- 約10秒で検温完了 ケースごと丸洗い可能なテルモの新型体温計
- 猛暑の夏を乗り切る! 冷却性能20%増の首元デバイスで−2℃体験へ
- 50万人の情報が流出した英国バイオバンクのインシデントでPETs利用は拡大するか
- ミカンの1種“タチバナ”にシミ抑制効果、メラニンの蓄積を阻害
- 細胞治療の調製から充填をシステムで自動化、品質のばらつき軽減へ
- キヤノンが医療ITをブランド統合、AI解析で新ソリューションの展開へ
- がんの微小病変解析をより正確に、1台で核酸抽出から定量を自動処理する装置
コーナーリンク



