すい臓がんの進行を抑制する遺伝子候補を発見:医療技術ニュース
東京理科大学は、脱リン酸化酵素CTDNEP1がすい臓がんのがん抑制遺伝子として機能する可能性を発見した。早期段階から発現量が低下し、生存率と密接に関連する。
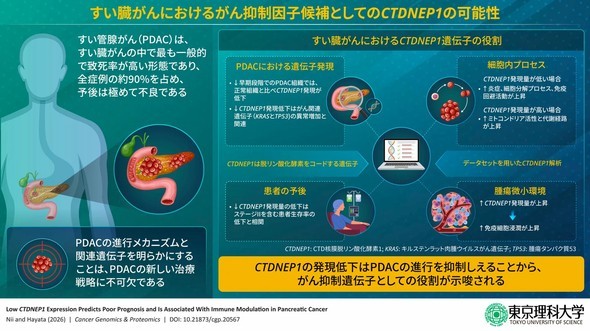
東京理科大学は2026年1月15日、脱リン酸化酵素CTDNEP1が、すい臓がんの進行を抑制するがん抑制遺伝子として機能している可能性を発見したと発表した。すい臓がん組織では正常組織と比較してCTDNEP1の発現量が低下しており、発現が低い患者ほど生存率が低いことが明らかとなった。すい臓がんの予後予測バイオマーカーや新規治療ターゲットとしての応用が期待される。
CTDNEP1は、これまで骨代謝や小児脳腫瘍への関与が知られている。今回の研究では、すい臓がんとの関連を調べるために、米国のがんゲノム研究データベース(The Cancer Genome Atlas:TCGA)に登録されているすい臓がん患者177例のサンプルデータを用いて相関解析を実施した。
解析の結果、すい臓がんではステージIの早期段階からCTDNEP1の発現が著しく低下していることが判明した。さらに、KRASなどすい臓がんの発生、進行に関与する遺伝子に異常がある腫瘍ほど、CTDNEP1の発現がより低くなる傾向が確認された。
予後との関連では、CTDNEP1低発現群の全生存率、疾患特異的生存率、無病生存率はCTDNEP1高発現群より有意に低下しており、特にステージIIの患者において顕著な差が見られた。
また、CTDNEP1低発現群では免疫および炎症反応やタンパク質分解に関わる経路が活性化している一方、CTDNEP1高発現群ではミトコンドリアの代謝やエネルギー産生に関わる経路やエネルギー代謝に関わる経路が活性化していた。
さらに、CTDNEP1の発現が高い腫瘍細胞では、CD4+T細胞やマクロファージなどの免疫細胞が腫瘍内に多く集まっていることが明らかとなった。これにより、CTDNEP1遺伝子の発現低下が免疫細胞の浸潤を減少させ、免疫逃避に関与している可能性が示唆された。
今後は、細胞や動物を用いた実験を通じて、CTDNEP1ががん細胞の増殖や転移に影響を与える詳細なメカニズムを検証する予定だ。
すい臓がんは初期の自覚症状が乏しく、発見時に進行している例が多い難治性がんだ。KRASやTP53といった既知の遺伝子異常だけでは進行メカニズムを十分に説明できず、重要な役割を果たす他の遺伝子の発見が求められていた。
関連記事
 がんを兵糧攻めで克服、「透明マント」技術で半減期を約10倍に
がんを兵糧攻めで克服、「透明マント」技術で半減期を約10倍に
ナノ医療イノベーションセンターらは、体内で100時間以上安定して働く新型ナノマシンを開発した。がん細胞の栄養を枯渇させる「兵糧攻め療法」で、膵がんと乳がんに高い治療効果を示した。 ロボットとAIで細胞医療の「死の谷」を克服、アステラスと安川出資の新会社が始動
ロボットとAIで細胞医療の「死の谷」を克服、アステラスと安川出資の新会社が始動
アステラス製薬と安川電機が共同出資するセラファ・バイオサイエンスが、ロボットとAIを活用して細胞医療製品の研究開発からGMP製造までを可能にする次世代細胞製造プラットフォームの事業展開について説明した。 レーザー加速によるイオン数の生成を最大10倍に拡大、がん治療装置小型化へ
レーザー加速によるイオン数の生成を最大10倍に拡大、がん治療装置小型化へ
量子科学技術研究開発機構は、レーザーで生成した高速イオンを、がん治療装置用に制御する技術を実証した。位相回転空胴を導入し、目的の速度のイオン個数を最大10倍ほど増やすことに成功した。 がん免疫療法が効かなくなるメカニズムを解明
がん免疫療法が効かなくなるメカニズムを解明
慶應義塾大学は、転移性尿路上皮がんの免疫チェックポイント阻害薬耐性の仕組みを解明した。がん細胞に繰り返し生じる遺伝子変異が多種の悪性サブクローンを生み、治療で克服しにくい免疫抑制環境を形成することが分かった。 オリンパスが内視鏡手術ロボット開発へ、米国で投資会社と新会社を設立
オリンパスが内視鏡手術ロボット開発へ、米国で投資会社と新会社を設立
オリンパスは、エンドルミナルロボティクスの開発を加速するため、米国の医療業界特化の投資会社であるリバイバルと契約を締結したと発表した。両社は同契約に基づき、米国に新会社「スワン・エンドサージカル(Swan EndoSurgical)」を共同で設立する。 がんの栄養経路を断つ新たな精密医療を開発
がんの栄養経路を断つ新たな精密医療を開発
大阪大学は、腫瘍組織の要となるニコチン酸アミドという代謝経路を標的とし、腫瘍の増殖を抑制する新たな分子標的薬を開発した。腫瘍微小環境を制御する新たな治療戦略となる。
関連リンク
Copyright © ITmedia, Inc. All Rights Reserved.
医療機器の記事ランキング
- 脳動脈瘤の治療をより安全に テルモが細径対応の新デバイス発売
- 約10秒で検温完了 ケースごと丸洗い可能なテルモの新型体温計
- 厚さ約25μmの神経シートを開発、光刺激と記録を同時に実現
- 知人より見知らぬ他人とシンクロ? スポーツ観戦の熱狂を科学的に解明
- 生きた乳酸菌は代謝、死んだ乳酸菌は免疫へ 状態で異なる腸内効果
- 日立ら肺がん細胞診の新解析技術 SEMと元素分析で検体評価を支援
- あなたの「網膜」は実年齢より老けている? 写真1枚でAIが疾患リスクを推定
- 50万人の情報が流出した英国バイオバンクのインシデントでPETs利用は拡大するか
- がんの微小病変解析をより正確に、1台で核酸抽出から定量を自動処理する装置
- 猛暑の夏を乗り切る! 冷却性能20%増の首元デバイスで−2℃体験へ
コーナーリンク