「次世代電池」はこれまでと何が変わるのか、何がスゴイのか:今こそ知りたい電池のあれこれ(21)(2/3 ページ)
次世代電池と従来のリチウムイオン電池を比較
次世代電池や革新電池の特徴を押さえるために、従来のリチウムイオン電池と比較して考えてみます。リチウムイオン電池と比べて、何が変わったからすごいのか? 何が革新的なのか? 同じ電池である以上は根本的には変わらない部分はどこか? そういった視点で、それぞれの電池の特徴を決定づける各要素について整理していきます。
変わらない点:化学電池かつ二次電池
酸化還元という化学反応を利用して電気的なエネルギーを取り出す「化学電池」であること。そして、その化学反応が可逆的であり、充電/放電という形で何度も繰り返し使うことができる「二次電池」であること。この2点については、リチウムイオン電池であろうと、次世代電池であろうと、どのような材料を用いて、どのような構造にしたとしても、同じ電池である以上は根本的には変わりません。
余談ですが、化学反応を伴わない物理電池を始め、その他にも電池という名称が用いられはするものの化学電池ではないデバイスもありますが、それらについてはまた別の機会に解説します。
変わる点:充放電に伴う化学反応自体の「反応機構」と「発生界面」
先述の通り、化学反応を利用して電気的なエネルギーを取り出すという電池としての根本的な仕組みや原理は変わりません。しかし、その化学反応がどのように進行するのかという「反応機構」と、どこで発生するのかという「発生界面」については、次世代電池や革新電池と呼ばれる電池系の多くにとって、リチウムイオン電池と比べて大きく変化した点であるといえるかと思います。
反応機構
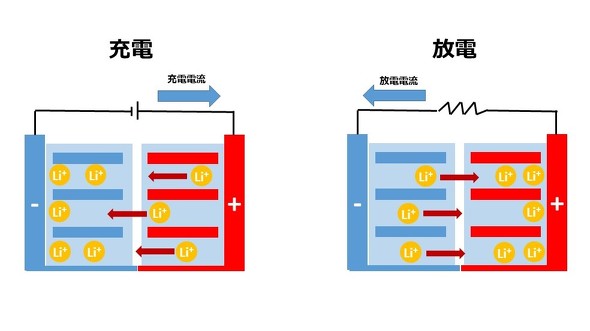
リチウムイオン電池の反応機構を説明する際、その特徴を表すものとして「ロッキングチェア」や「インターカレーション」という言葉がしばしば用いられます。
「ロッキングチェア」(揺り椅子)という名が示すのは、電解液中のリチウムイオンの動き方です。揺れては戻ると繰り返し、振り子のように何度も何度も左右に行ったり来たりするロッキングチェアのように、充電の際はリチウムイオンが正極から負極へ、放電の際は負極から正極へと、充放電に伴ってリチウムイオンが行ったり来たりする反応のことを「ロッキングチェア型」の反応と呼びます。このようにイオンが行ったり来たりする動きを表現するものとして「シーソー型」や「シャトルコック型」と呼ばれることもあります。
鉛蓄電池などの従来電池の多くは充放電に伴って電極材料の溶解析出を繰り返すため、反応生成物の蓄積や電解液中のイオン濃度変化が発生するのに対し、ロッキングチェア型の場合は同じイオンが行ったり来たりするだけで大きな変化は生じず、電池全体の構成で考えると必要な電解液量が少なくなるという特徴もあります。
一方、「インターカレーション」というのは、リチウムイオン電池の反応機構を電極構造に着目した場合の表現です。
先ほども述べたように、鉛蓄電池などの従来電池の多くは電極材料が充電/放電を繰り返すとともに、電極材料が溶解と析出を繰り返すことになります。このとき、一度溶解した電極材料が必ずしも電極上の同じ箇所に再析出するとは限らず、充放電を繰り返すたびに電極の形状が変化し、最悪の場合、針状に成長した電極材料による内部短絡が生じる可能性もあります。
それに対してリチウムイオン電池のような「インターカレーション型」の反応の場合、電極材料自体は溶解析出といった大きな変化はせず、構造内部へのリチウムイオンの脱離と挿入を繰り返すことで進行します。その挙動から、挿入を意味する「インサーション型」と呼ばれることもあります。
「ロッキングチェア」「インターカレーション」といった反応機構は、電極や電解液に大きな変化を伴わずに安定した充放電を繰り返すことができるというリチウムイオン電池の優れた電池特性を生み出す一因でもありましたが、その一方で達成可能なエネルギー密度に理論的な制約が生じるという側面もありました。
そこで、より高いエネルギー密度を達成するため、電極や電解液の化学的な変化を許容する「リザーバ型」という仕組みの検討がなされています。
単体金属を負極に用いる「金属電池」など、電極材料が充放電によって溶解析出を繰り返す従来電池の反応機構に立ち戻ることでエネルギー密度を向上させつつ、課題であった耐久性や安全性を改善するために最新の技術を駆使した取り組みが進められています。
Copyright © ITmedia, Inc. All Rights Reserved.
モビリティの記事ランキング
- 新型「bZ4X」の走行距離が伸びた理由、デンソーの「世界初」と「世界最高」が貢献
- ギガキャストを発案したテスラの現在・過去・未来
- ECUの一体化で進化したトヨタの「新型TSS」 RAV4の安全走行を支える技術とは
- スズキ、排出ガス中のCO2を回収し農場で再利用できる「スーパーキャリイ」披露
- どこへでも移動可能な自由を── ランドクルーザーの新型車「FJ」シリーズが登場
- SDV時代には「製品開発スピード」だけでなく「製品発見スピード」も求められる
- 「新興勢力に圧倒的に劣っている」――ホンダは開発を根本から変えられるか
- コマツが次世代月面物流ローバーの研究開発を開始
- 新型「CX-5」はSUVの王道を極める、SDV化も進みアップデートでGeminiも利用可能
- 4kWhバッテリー搭載電動バイク「L-noa」 大手4社に原付一種で挑む理由
コーナーリンク