「Apple Watch Series 4」の心電図アプリはFDA認証をどうやって取得したのか:海外医療技術トレンド(39)(3/3 ページ)
グローバルプラットフォーマーのウェアラブル型医療機器市場参入の裏側には、規制当局からイノベーション当局へのトランスフォーメーションをめざすFDAの政策がある。
アップルも参画するFDAのデジタルヘルスPre-Certプログラム
アップルが「Apple Watch Series 4」の新製品発表を行ったのと同じ9月12日、FDA長官のスコット・ゴットリーブ氏と医療機器・放射線保健センター長のジェフリー・シューレン氏は、デジタルヘルス・イノベーションに関する声明を発表した(関連情報)。
この声明では、本連載第27回で取り上げた「デジタルヘルス・イノベーション行動計画」(関連情報、PDF)や、「デジタルヘルスソフトウェア事前認証(Pre-Cert)プログラム」(関連情報)に触れている。
参考までにFDAは、2017年9月26日、デジタルヘルスのソフトウェア事前認証パイロットプログラムの参画企業として、アップルを含む下記9社(米国企業7社、外国企業2社)を公表している。
- アップル(カリフォルニア州クパチーノ)
- フィットビット(カリフォルニア州サンフランシスコ)
- ジョンソン・エンド・ジョンソン(ニュージャージー州ニューブランズウィック)
- ペア・セラピューティクス(マサチューセッツ州ボストン)
- フォスフォラス(ニューヨーク州ニューヨーク)
- ロシュ(スイス・バーゼル)
- サムスン電子(韓国・ソウル)
- タイドプール(カリフォルニア州パロアルト)
- ベリリー(カリフォルニア州マウンテンビュー)
また、図2は、FDAが2018年6月に公表した「ソフトウェア事前認証プログラムの構築−作業モデル[v0.2]」の構成要素を示しており、下記4項目が柱となっている。
- 卓越性の評価と事前認証
- レビュー経路の決定
- 簡素化された市販前レビュープロセス
- リアルワールド・パフォーマンス
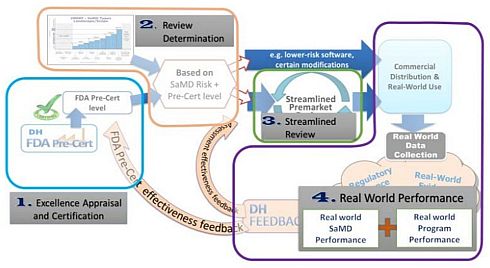
図2 FDA「ソフトウェア事前認証プログラムの構築−作業モデル[v0.2]」の構成要素(クリックで拡大) 出典:FDA「Developing Software Precertification Program: Working Model - Version 0.2」(2018年6月)
このうち、「4.リアルワールド・パフォーマンス」に関連して、FDAは2019年のテストフェーズに向けて、図3のような「リアルワールド・パフォーマンス分析(RWPA)」のフレームワークを提案している。
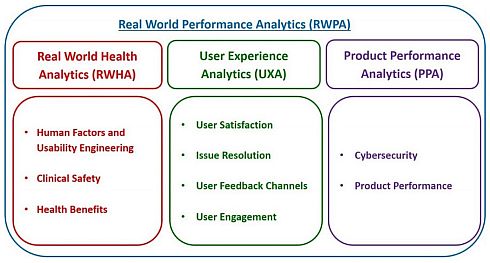
図3 リアルワールド・パフォーマンス分析のフレームワーク(クリックで拡大)(クリックで拡大) 出典:FDA「Developing Software Precertification Program: Working Model - Version 0.2」(2018年6月)
リアルワールド・パフォーマンス分析は、「リアルワールド・ヘルス分析(RWHA)」「ユーザーエクスペリエンス分析(UXA)」「製品パフォーマンス分析(PPA)」から構成される。ユーザーエクスペリエンス分析に、ゲーミフィケーション技術の適用と関わりの深い「ユーザーエンゲージメント」が組み込まれ、製品パフォーマンス分析に、医療機器の市販後安全対策で課題となっている「サイバーセキュリティ」が組み込まれるなど、注目すべき点が多い。
デジタルヘルスを起点とするレギュラトリーサイエンス研究体制再構築
FDAの声明では、2019会計年度予算より、「センター・オブ・エクセレンス・フォー・デジタルヘルス」の創設計画について言及している。FDAは、新たなセンターに関連して、より効率的な規制パラダイムの創設、第三者認証機関を評価・認定する機能の構築に向けた検討、ソフトウェアベースの機器の進化を補うサイバーセキュリティ部門の支援などの方向性を示しており、今後の動向が注目される。
参考までに、FDAが2018年2月13日に公表した2019会計年度予算要求では、以下のような項目が掲げられていた(関連情報)。
- 国内生産の促進:効率的な規制経路の開発を通じた現代的な医薬品・生物学的製剤製造技術の促進
- 新たな国内医薬品産業の進歩と、化合物製品の堅牢で信頼できるソースとしてのアウトソーシング機能セクターの創設によるアクセスの促進
- MedTech製造を内部へ:医療機器の製造と品質の促進
- 新たな医療データ企業の創出:人間と動物の健康を改善し、市販前評価と市販後安全をっ支援するためのリアルワールドエビデンス利用の促進
- 規制を、信頼できる市販後監視のための効率的で斬新なフレームワークにシフトすることによって、デジタルヘルス技術産業の成長を促進し、トランスフォメーションを加速させる
- 政府機関が、現代科学に基づく新薬開発の原則をより効率的に開発・評価し、この情報をイノベーターと共有するための方法に関する新たなプラットフォームの構築
- 希少性疾患を標的とする医療製品の投資、イノベーションの刺激
- ジェネリック医薬品開発の現代化と、競争力の強化を可能にするレビュー、ジェネリック医薬品の代用の促進、米国の患者のための入手可能な選択肢の提供
今秋の米国中間選挙を経て、トランプ政権が2019年以降どのような形でデジタルヘルス推進政策を展開していくのかが注目される。
筆者プロフィール
笹原英司(ささはら えいじ)(NPO法人ヘルスケアクラウド研究会・理事)
宮崎県出身。千葉大学大学院医学薬学府博士課程修了(医薬学博士)。デジタルマーケティング全般(B2B/B2C)および健康医療/介護福祉/ライフサイエンス業界のガバナンス/リスク/コンプライアンス関連調査研究/コンサルティング実績を有し、クラウドセキュリティアライアンス、在日米国商工会議所等でビッグデータのセキュリティに関する啓発活動を行っている。
Twitter:https://twitter.com/esasahara
LinkedIn:https://www.linkedin.com/in/esasahara
Facebook:https://www.facebook.com/esasahara
Copyright © ITmedia, Inc. All Rights Reserved.
関連記事
- 連載「海外医療技術トレンド」バックナンバー
 スマートウォッチの差別化は薬事法・FDA対応に、手首式血圧計を2018年発売
スマートウォッチの差別化は薬事法・FDA対応に、手首式血圧計を2018年発売
オムロン ヘルスケアは、消費者向けエレクトロニクス展示会「CES 2018」において、手首で測定するスマートウォッチ型の血圧計を出展する。 米国医療界がグーグルやアップルと連携を深める理由は「相互運用性の標準化」
米国医療界がグーグルやアップルと連携を深める理由は「相互運用性の標準化」
モバイルヘルスやデジタルヘルス機器の普及に積極的な米国の医療界では、グローバルプラットフォーマーとの連携強化が本格化している。その背景には「相互運用性の標準化」がある。 リアルワールドエビデンスに基づく医療機器開発の時代へ
リアルワールドエビデンスに基づく医療機器開発の時代へ
米国では「21世紀医療法」に基づく医療イノベーション推進策が本格化しており、ヘルスデータ利活用の領域まで及んでいる。そこで重視されているのが「リアルワールドデータ(RWD)」と「リアルワールドエビデンス(RWE)」だ。 トランプ政権下でも着々と進む米国のデジタルヘルス規制の枠組みづくり
トランプ政権下でも着々と進む米国のデジタルヘルス規制の枠組みづくり
「医療機器」と「非医療機器」の双方に重なり合うデジタルヘルス。米国では、イノベーション促進に向けた規制の枠組みづくりが本格化している。 米国FDAが強化を求める医療機器のサイバーセキュリティ
米国FDAが強化を求める医療機器のサイバーセキュリティ
重要情報インフラの中でも、サイバー攻撃による脅威の拡大が顕在化している米国の医療界。医療のICTサプライチェーンを担う医療機器企業に対するセキュリティの要求事項も高度化している。