生体内のがん組織を指紋認証のように識別する標識化技術を開発:医療技術ニュース
理化学研究所は、細胞上で人工糖ペプチドを合成することで、指紋認証のようにがん細胞をパターン認識し、そのパターンを利用してマウス体内で特定のがん組織を標識化することに成功した。
理化学研究所は2020年3月9日、細胞上で人工糖ペプチドを合成することで、指紋認証のようにがん細胞をパターン認識し、そのパターンを利用してマウス体内で特定のがん組織を標識化することに成功したと発表した。同研究所開拓研究本部主任研究員 田中克典氏らの研究チームによる成果だ。
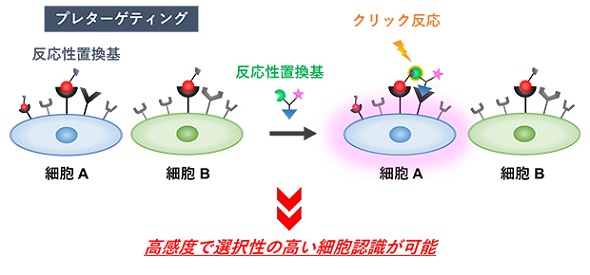
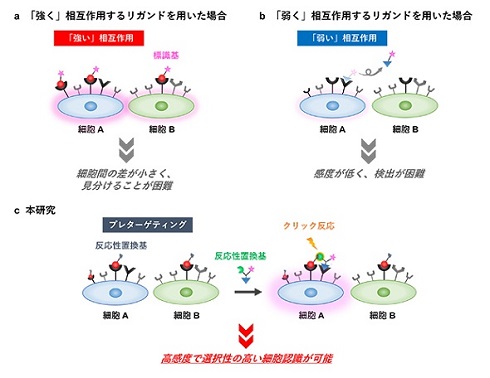
田中氏らは2017年に、強弱2つの相互作用を利用する細胞認識技術を開発している。細胞上の受容体に、強く相互作用するペプチドリガンドを一次的に相互作用させた後(プレターゲティング)に、弱く相互作用する糖鎖リガンドを同じ細胞上の別の受容体に二次的に相互作用させる。糖鎖リガンドには、ペプチドリガンドと選択的に結合する反応性官能基と標識基が結合しているため、2種類の受容体が存在する細胞上でのみ糖ペプチドが生成され、糖鎖リガンドの標識基を検出できるというものだ。
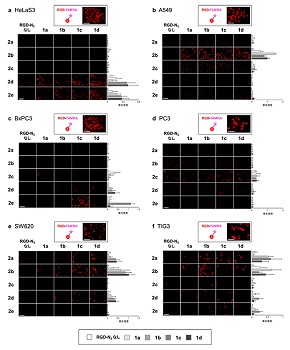
研究チームは今回、この細胞認識技術の一般化を試みた。強く相互作用するペプチドリガンドを4種、弱く相互作用する糖鎖リガンドを5種類用いて、ヒト子宮頸がん細胞「HeLaS3」やヒト肺胞基底上皮腺がん細胞「A549」など5種のがん細胞と、非がん細胞であるヒト二倍体線維芽細胞「TIG3」1種に応用。相互作用が強いものと弱いもの、2種類のリガンドを組み合わせることで、がん細胞と非がん細胞のパターン認識に成功した。
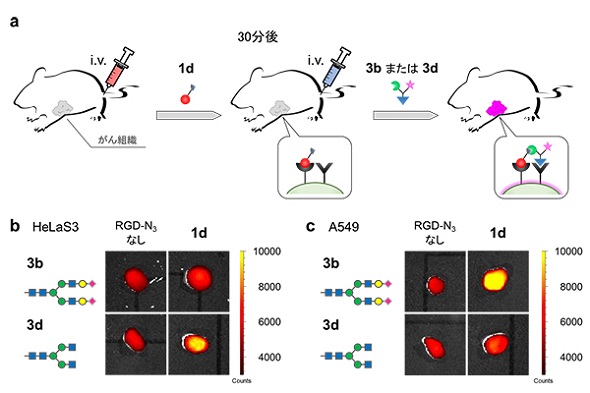
続いて、この方法をマウスの生体内で展開した。がん細胞を播種したマウスにペプチドリガンドを投与し、その30分後に糖鎖リガンド(3b、3d)を投与して、がん組織を標識した。その結果、HeLaS3由来のがん組織では3dに、A549由来の組織では3bで強い蛍光シグナルが検出され、がん組織を選択的に見分けることができた。
従来の生体内分子イメージングでは、標的細胞表面の1種類の受容体に強く相互作用するリガンドが用いられてきた。しかし、この手法では、標的細胞以外の受容体にも強く相互作用してしまうため、感度良く見分けることは困難だった。また、弱い相互作用のリガンドのみでは、相互作用してもすぐに離れてしまうため、検出に利用できなかった。
今回の成果は、生体内のがん組織や疾患部位を選択的に識別する新たな診断方法の開発につながることが期待される。
Copyright © ITmedia, Inc. All Rights Reserved.
関連記事
 小細胞肺がんに近赤外光線免疫療法を適用し、効果を確認
小細胞肺がんに近赤外光線免疫療法を適用し、効果を確認
名古屋大学が、タンパク質DLL3を分子標的とする小細胞肺がんの近赤外光線免疫療法を発表した。細胞実験と動物実験において、DLL3を標的とした小細胞肺がんに対する効果が確認できた。 液体のりの主成分を利用し、第5のがん治療法の効果を向上
液体のりの主成分を利用し、第5のがん治療法の効果を向上
東京工業大学は、液体のりの主成分をホウ素化合物に加えることで、ホウ素中性子捕捉療法の治療成果が大幅に向上することを発見した。マウスの皮下腫瘍に対する治療効果は、ほぼ根治レベルだった。 細胞が移動する方向を予測するAIを開発、がんの予後診断に期待
細胞が移動する方向を予測するAIを開発、がんの予後診断に期待
慶應義塾大学は、現在の細胞の画像から、細胞がどの方向に移動するかを予測できるAIを開発した。がんの予後診断など、未来の予測が強く要求される医療分野への応用が期待される。 食とがん発症の関係性の研究がAI技術開発事業のテーマに採択
食とがん発症の関係性の研究がAI技術開発事業のテーマに採択
キユーピーは、横浜国立大学、東京医科大学と共同で、新エネルギー・産業技術総合開発機構の「次世代人工知能・ロボット中核技術開発」プロジェクトに応募し、AIの信頼性に関する技術開発事業に採択された。 次世代がん遺伝子パネルに関する共同研究開発を開始
次世代がん遺伝子パネルに関する共同研究開発を開始
東京大学はコニカミノルタおよび国立がん研究センター研究所と共同で、DNAとRNAを解析する東大オンコパネルを基盤とし、遺伝子診断技術の知見を融合させる研究を進め、次世代包括的がん遺伝子パネル検査を開発する。