再生医療用セラミックス製品に関する世界初の国際規格:医療機器ニュース
物質・材料研究機構の職員が提案した、再生医療用セラミックス製品の評価法に対して、世界初の国際規格が発行された。再生医療用セラミックス製品の評価の一部を適正かつ簡便に進めることができ、動物を用いないため動物愛護にも寄与する。
物質・材料研究機構(NIMS)は2018年4月25日、NIMS職員が提案した再生医療用セラミックス製品の評価法について、世界初の国際規格が発行されたと発表した。
発行された国際規格は、細胞外マトリックスの骨の再生に使用される、生体活性の高いバイオセラミックス多孔体の評価手法や評価基準に関するものだ。バイオセラミックスの評価法については、動物実験を細胞実験に代替する手法が求められていたが、これまで国際標準となる試験法はなかった。
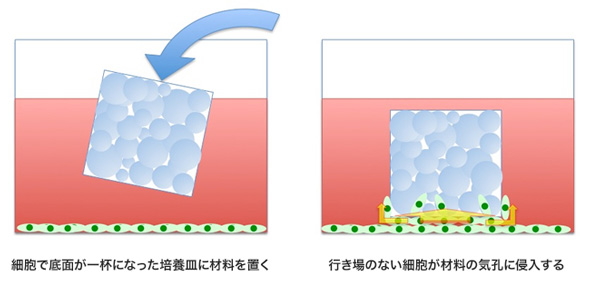
今回、NIMSバイオセラミックスグループ リーダーの菊池正紀氏が、従来にない発想の試験法を発案した。セラミックス多孔体中への細胞の入り込みやすさを測定するもので、産業技術総合研究所や大学、メーカーと検討したところ、同手法が動物実験におけるバイオセラミックス多孔体内での骨形成と相関性を持つことが分かった。
その妥当性を、イギリスやスイスの大学とともに国際ラウンドロビンテストで確認し、2013年4月にISO(国際標準化機構)、TC150(外科用インプラント)、SC7(再生医療機器)、WG3(骨格組織用再生医療機器)に提案した。その後、菊池氏が各国専門家からの意見をすり合わせた結果、2018年1月17日にISO、TC150、SC7では初となる国際規格ISO 19090として発行された。
同規格の発行により、動物を用いずに再生医療用セラミックス製品の評価の一部を適正かつ簡便に進めることができ、動物愛護にも寄与する。また、この試験法は、セラミックス以外の金属やポリマーからなる再生医療製品の評価法としても応用できるため、迅速な材料開発に貢献する。
*** 一部省略されたコンテンツがあります。PC版でご覧ください。 ***
Copyright © ITmedia, Inc. All Rights Reserved.
関連記事
 従来比6万倍の速さで自己修復するセラミックス、人間の骨と同じ治り方だった
従来比6万倍の速さで自己修復するセラミックス、人間の骨と同じ治り方だった
物質・材料研究機構は、自己修復するセラミックスの修復速度が最速で従来比6万倍になり、発生した亀裂を1分で修復できる技術を開発。航空機エンジンのタービンなどに用いられている金属材料をセラミックスに代替でき、大幅な軽量化によるCO2排出量の削減につなげられるという。その修復プロセスは、人間の骨と同じだった。 あなたの骨を3Dプリンタで作ります、細胞増殖が可能な人工骨
あなたの骨を3Dプリンタで作ります、細胞増殖が可能な人工骨
理化学研究所とリコーは、3Dプリンタを用いて、患者の骨の内部を含む欠損部位の形状を再現する手法を開発した。作製した3次元造形人工骨は、数分間水洗いすれば細胞が増殖できる状態になり、強度や骨置換性に優れていることが分かった。 3Dプリンタで成形する「カスタムメイド人工骨」をEU諸国で製造・販売
3Dプリンタで成形する「カスタムメイド人工骨」をEU諸国で製造・販売
NEDOプロジェクトにおいて、3Dプリンタで成形するカスタムメイド人工骨CTボーンを開発したネクスト21が、2015年4月30日にオランダXillocとEU諸国における製造・販売に関するライセンス契約を締結した。 骨髄の空洞を維持する遺伝子が見つかる、再生医療や骨粗しょう症治療に期待
骨髄の空洞を維持する遺伝子が見つかる、再生医療や骨粗しょう症治療に期待
大阪大学は、間葉系幹細胞で発現する転写因子Ebf3が、血液細胞の工場である骨髄腔を維持し、血液細胞を育てる微小環境を作っていることを明らかにした。 歯科のインプラント治療で使用可能な人工骨、歯の無機成分と同じ組成
歯科のインプラント治療で使用可能な人工骨、歯の無機成分と同じ組成
九州大学とジーシーは、骨の無機成分と同組成の人工骨を開発し、歯科用インプラント治療で使用可能な人工骨として国内初の薬事承認を得た。これにより治療時の患者への侵襲を伴う自家骨採取が不要になる。