脳の働きに重要なIP3受容体の動作原理を解明、神経疾患や認知症の治療に貢献:医療技術ニュース
理化学研究所は、記憶や学習などの脳機能に必要なIP3受容体の動作原理を、X線結晶構造解析と変異体の機能解析によって解明した。今後、神経疾患や認知症の治療/予防に役立つことが期待される。
理化学研究所は2017年4月18日、記憶や学習などの脳機能に必要なIP3受容体(イノシトール三リン酸受容体)の動作原理を解明したと発表した。同研究所 脳科学総合研究センター 研究員の濱田耕造氏とチームリーダーの御子柴克彦氏らの共同研究チームによるもので、成果は同月17日、米科学誌「Proceedings of the National Academy of Sciences of the United States of America(PNAS)」電子版に掲載された。
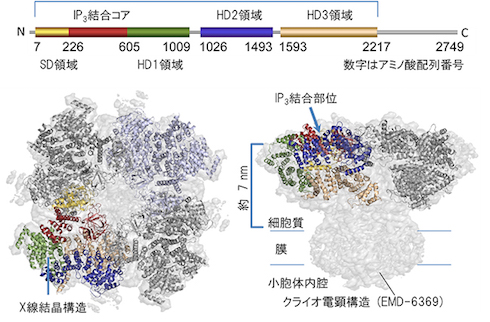
直径約20nmのIP3受容体は、小胞体の膜上に局在するタンパク質。個体の発生や、神経のシナプス(接点)における情報伝達効率の変化に関わっている。IP3受容体が4つ組み合わさることで、中心部にカルシウムイオン(Ca2+)を1つだけ通す小さなイオン透過口を形成し、カルシウムチャネルとして働く。
IP3受容体は、リガンド(受容体に結合する物質)であるIP3を特異的に認識し結合させ、Ca2+を放出する。従来は、チャネル部位に近いIP3結合部位から直接チャネル部位へ構造変化が伝達されることでチャネルが開くという動作モデルが考えられていた。しかし、既知のリガンド作動型イオンチャネルに比べ、IP3結合部位はチャネル部位から大きく(7nm以上)離れているため、IP3が物理的にどのようにチャネルを開けるのかは不明だった。
同研究チームは今回、遺伝子工学を用いて、IP3結合部位からチャネル部位につながるタンパク質結晶を大量に作製。その立体構造を大型放射光施設「SPring-8」を使ってX線結晶構造解析し、決定することに成功した。これまでに知られている通り、IP3結合部位からチャネル部位までが約7nm離れていることを確認した。
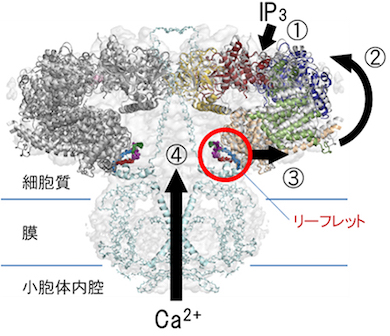
さらに、IP3存在下・非存在下と欠失変異体の結晶構造も決定。IP3が結合して生じる構造変化の経路を見いだし、IP3が受容体に結合してからチャネルを開けるまでの動作原理を解明した。
IP3受容体の遺伝子に突然変異が起こると、家族性脊髄小脳失調症やGillespie(ガレスピー)症候群を発症する。また、認知症の主な原因とされる神経変性にIP3受容体が関わることも知られている。そのため、IP3受容体の動作原理の解明は、これらの病気の治療薬や予防法の開発にもつながると考えられていた。今回明らかにされた機構は、今後、神経疾患や認知症の治療や予防に役立つ新しい創薬ターゲットとして期待される。
Copyright © ITmedia, Inc. All Rights Reserved.
関連記事
 認知症の一種、前頭側頭葉変性症(FTLD)の発症メカニズムを解明
認知症の一種、前頭側頭葉変性症(FTLD)の発症メカニズムを解明
名古屋大学は、若年性認知症の2割弱を占めるといわれる前頭側頭葉変性症(FTLD)が発症するメカニズムを解明した。RNAタンパク質のFUSやSFPQの機能喪失マウスモデルでは、FTLDに類似する高次機能障害が起こることを確認した。 従来比3倍の感度を備えたヘルメット型PETを開発、認知症の早期診断に期待
従来比3倍の感度を備えたヘルメット型PETを開発、認知症の早期診断に期待
放射線医学総合研究所とアトックスの共同研究チームは、従来比3倍の感度を備えたヘルメット型PETを開発した。微量な原因タンパク質の画像化が可能になることで、認知症の早期診断が期待される。 認知症予防の脳トレサービス開発に日立が協力
認知症予防の脳トレサービス開発に日立が協力
日立ハイテクノロジーズと日立製作所は、キッズスターが提供する高齢者向け認知症・介護予防サービス「脳エクササイズ」の開発に協力し、Brain Scienceマークを付与した。 アルツハイマー型認知症の記憶障害メカニズムに関する新発見
アルツハイマー型認知症の記憶障害メカニズムに関する新発見
広島大学は、標的とした神経細胞のみを取り除く技術を利用して、前脳基底部からアセチルコリン神経細胞を除去することに成功、異なるタイプのアセチルコリン神経細胞が別々の再認記憶の機能を担っていることを初めて明らかにした。 がんや認知症を健診で簡単に発見、産官学共同で次世代診断システム開発へ
がんや認知症を健診で簡単に発見、産官学共同で次世代診断システム開発へ
新エネルギー・産業総合開発機構(NEDO)は、国立がん研究センター(以下、NCC)や東レなどが、健康診断などで簡単にがんや認知症を検査できる診断システムの開発プロジェクトを発表した。「マイクロRNA」と呼ばれるバイオマーカーを使って、1度の採血で13種類のがんを診断できるシステムの実用化を目指す。