医薬品医療機器等法(薬機法)の全体像を俯瞰する:医療機器開発のための薬機法解説(1)(3/3 ページ)
2014年11月に施行された医薬品医療機器等法は、従来の薬事法と比べて医療機器の開発に関わる部分で大きな改正が行われた。本連載では「薬機法」の略称で呼ばれている同法について医療機器開発の観点から解説していく。第1回では、改正前の薬事法との比較から薬機法の全体像を俯瞰する。
5)医療機器の分類
記事の冒頭で、医療機器の製品範囲は意外に広いという話をしましたが、一言で「医療機器」と言っても、比較的安全な物から人の命に直結する物まで、さまざまな種類があります。
そして医療機器に関する規制としては、2000年代に入ってからの薬事法の法改正で「リスクに応じたクラス分類制度が導入された」ことも挙げました。
このように、医療機器はリスク※)の程度(副作用または機能の障害が生じた場合において、人の生命および健康に影響を及ぼす程度)によって、分類されています。
※)ここで言うリスクとは、人に対して適正に使用したときのリスクに限られます。
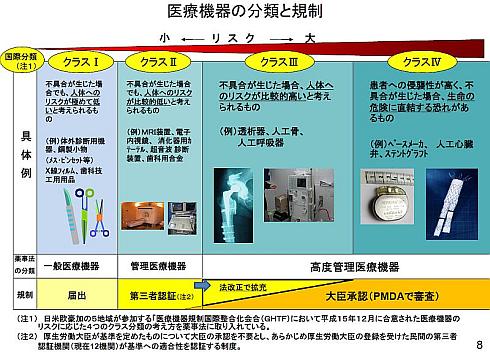
このクラス分類は、主に以下の観点によりチェックされ、リスクの程度により「一般医療機器」「管理医療機器」「高度管理医療機器」に分類されます。
- 生体への接触部位
- 生体への接触時間
- 不具合が生じた場合の危険性の大きさ
また、国内のリスク分類に対応した国際分類(リスクI〜リスクIV)もありますので、併せて以下の図で示します。
※)「侵襲性」とは、身体に及ぼす物理的負担や影響の大きさのことを指します。
さて、連載の第1回では、薬事法から医薬品医療機器等法への改正の全体像と医療機器という分野の概要について書きました。次回からは、トピックを絞りながら医療機器開発にまつわる医薬品医療機器等法についての解説を進めていきます。お楽しみに!
筆者プロフィール
吉田 武史(よしだ たけし)/吉田法務事務所 代表、日本薬事法務学会 理事長
東京理科大学薬学部在学時から行政書士として吉田法務事務所を開業。その後、薬剤師の国家試験にも合格し、行政書士の法律知識と薬剤師の薬学知識とを活かした活動を行っている。医療機器や化粧品、医薬部外品など薬機法に関わる行政照会の実績を多数持ち、クライアントの悩みを解消する薬事法務関連のコンサルティング業務を得意としている。
http://www.yakuji.net/
http://www.japal.org/
Copyright © ITmedia, Inc. All Rights Reserved.
関連記事
 「伴走コンサル」で“売れる”医療機器の開発につなげたい
「伴走コンサル」で“売れる”医療機器の開発につなげたい
2014年後半から2015年にかけて、日本政府から医療機器の開発を支援するための施策が続々と進められている。これらの施策の立案と実施に携わっている、経済産業省の商務情報政策局で医療・福祉機器産業室長を務める土屋博史氏に話を聞いた。 米国の事例に見る、マルチデバイス化する「非医療機器」のリスク管理
米国の事例に見る、マルチデバイス化する「非医療機器」のリスク管理
近年、健康増進用途の消費者向けウェアラブル端末やモバイルソフトウェアなど、医薬品医療機器等法(薬機法)の適用対象外となる「非医療機器」のマルチデバイス化が進んでいる。それに伴ってどのようなリスクが出てくるのか。米国の動向をみてみよう。 米国FDAが強化を求める医療機器のサイバーセキュリティ
米国FDAが強化を求める医療機器のサイバーセキュリティ
重要情報インフラの中でも、サイバー攻撃による脅威の拡大が顕在化している米国の医療界。医療のICTサプライチェーンを担う医療機器企業に対するセキュリティの要求事項も高度化している。 「薬事認証の国際協調を進める」、厚労省が新戦略「RSI」を策定中
「薬事認証の国際協調を進める」、厚労省が新戦略「RSI」を策定中
「第6回 医療機器 開発・製造展(MEDIX2015)」の特別講演に、厚生労働省の大臣官房参事官(医療機器・再生医療等製品審査管理担当)を務める磯部総一郎氏が登壇。現在準備を進めている新たな政策を明らかにした。 ロボット治療器「HAL」が8カ月で薬事承認を取得、次は保険適用を目指す
ロボット治療器「HAL」が8カ月で薬事承認を取得、次は保険適用を目指す
サイバーダインは、同社のロボット治療器「HAL医療用下肢タイプ」が厚生労働省から医療機器の製造販売承認を取得したと発表した。今後は公的医療保険の適用に向けた準備を進める。