医薬品医療機器等法(薬機法)の全体像を俯瞰する:医療機器開発のための薬機法解説(1)(2/3 ページ)
2014年11月に施行された医薬品医療機器等法は、従来の薬事法と比べて医療機器の開発に関わる部分で大きな改正が行われた。本連載では「薬機法」の略称で呼ばれている同法について医療機器開発の観点から解説していく。第1回では、改正前の薬事法との比較から薬機法の全体像を俯瞰する。
3)「医薬品医療機器等法」改正のポイント
厚生労働省では「薬事法等の一部を改正する法律の概要」として、以下の3つのポイントをあげています。
- 医薬品、医療機器等に係る安全対策の強化
- 医療機器の特性を踏まえた規制の構築
- 再生医療等製品の特性を踏まえた規制の構築
1)については、大きな薬害事件、主に薬害肝炎の事件を通して、「添付文書」を最新なものに常に保つようにすることと、それらをWebサイトなどを通じて公開するようにし、安全性を常に確保、検証していく体制をとるということが大きなポイントとなっています。
「添付文書」とは、簡単に言ってしまえば説明書のようなものです(PMDA(独立行政法人医薬品医療機器総合機構)医療機器の添付文書情報検索ページ)。
3)には、今後開発や実用化が進んでいくであろう、新たな分野である「再生医療」に関連する製品などの決まりごとを整備したものです。
そして、本連載のテーマとなる医療機器が出てくるのが2)、「医療機器の特性を踏まえた規制の構築」というものです。
厚生労働省は、同じ資料でこの医療機器に関する改正の背景を次のように書いています。
- 医療機器は、PC等の他の機械製品と同様に短いサイクルで改善・改良が行われた製品が市場に供給される場合が多いことなど、医薬品と異なる特性を有している
- 新医療機器の開発・実用化については、医療の質の向上に寄与するとともに、我が国の経済成長をけん引する産業分野としても期待されているが、承認・上市に時間がかかる等といった課題も指摘
- さらに、医療機器の国際展開を進めるためには、国際整合性に配慮する必要がある
- このため、医療機器の特性を踏まえた制度改正を行い、医療機器の迅速な実用化と規制の合理化を図ることが必要
最初に、医薬品、つまり“お薬”と医療機器は異なる特性を持っている、ということを認識して法律を整備することをうたっています。
その違いとしては、
- 臨床現場での実際の使用を通じて、実用化されること
- 絶えず改良・改善が行われ、一製品あたりの寿命が短いこと
- 有効性・安全性は、医師等の技能に依る部分が大きく、かつ、臨床現場では少量多品目が使用されていること
などを挙げています。
つまり医療機器とは、ある程度専門性を持った人間が使用する機械であり、先端技術開発を含め常に改良が行われることで、製品ライフサイクルが短く、医療現場での実地試験を経て実用化されるものである、としているのです。
次に、この分野が日本という国の経済成長に寄与する分野であるという認識を示しています。それと同時に、先出の「デバイスラグ」の問題が指摘されていることをうたっています。
そして、この成長分野として期待する医療機器を海外にも展開させるために「国際整合性への配慮」いわゆるグローバルハーモナイゼーションが必要であるとしています。ISOやCEマーキングなど国際的な標準の考え方を取り入れて、これらを法改正に適用することで、法律としての決まりごとを分かりやすくし、機器の実用化を加速させることを趣旨としている、というわけです。
4)そもそも医療機器とは?
ここまで法改正の概要について書きましたが、肝心の「医療機器」について知るに当たり、まずはどのようなものが医療機器に該当するのかを確認しましょう。
医薬品医療機器等法によると、医療機器は「使用目的」「形態」「政令」の3つの観点から定義されます。
| 使用目的 | ・人又は動物の疾病の診断、治療又は予防に使用される |
|---|---|
| ・人又は動物の身体の構造又は機能に影響を及ぼす | |
| 形態 | 機械器具としての形態を持つこと。なお、歯科材料、医療用品及び衛生用品は、社会通念上、機械器具とは認めがたいものの、医薬品医療機器等法においては、機械器具“等”として同じ取扱いをする |
| 政令 | 個々の物が政令により指令される。政令では次のものが定められています |
| ・機械器具…84のもの | |
| ・医療用品…6のもの | |
| ・歯科材料…9のもの | |
| ・衛生用品…4のもの | |
| ・プログラム…3のもの | |
| ・プログラムを記録した記録媒体…3のもの | |
| ・動物専用医療機器…14のもの | |
| 表 医療機器は「使用目的」「形態」「政令」の3つの観点で定義される | |
これらの中で、今回の改正で大きく変わったのは「プログラム」に関する部分です。
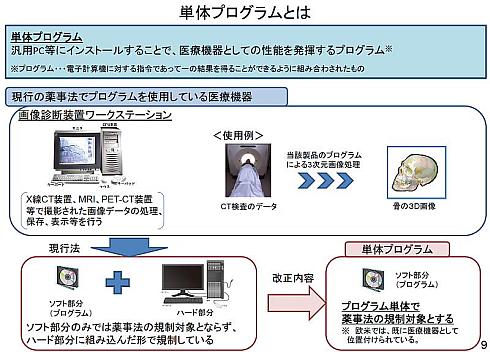
これまでは、ソフトウェア(プログラム)だけでは医療機器にならず、ソフトウェア+ハードウェアとなる場合に医療機器とされていました。しかし新法では、ソフトウェア単体でも医療機器として扱われるようになりました。
これを「単体プログラム」「医療機器プログラム」などと呼んでいます。
Copyright © ITmedia, Inc. All Rights Reserved.