ゲノム編集を青色の光で自在に制御する技術を開発:医療技術ニュース
東京大学は、「ゲノム編集」と呼ばれる遺伝子の改変操作を、光で自在に制御する技術を開発した。光スイッチタンパク質を用いることで、CRISPR-Cas9システムのDNA切断酵素の活性を青色の光で制御した。
東京大学は2015年6月17日、「ゲノム編集」と呼ばれる遺伝子の改変操作を、光で自在に制御する技術を開発したと発表した。同大大学院総合文化研究科の二本垣裕太大学院生と佐藤守俊准教授らの研究グループによるもので、6月15日に米科学誌「Nature Biotechnology」の電子版に掲載された。
原核生物で発見されたCRISPR-Cas9システムに基づくゲノム編集技術は、ゲノム上の狙った遺伝子の機能を破壊(ノックアウト)したり、別の塩基配列に置き換える(ノックイン)ことができる。ゲノム編集には、ゲノム上の狙った塩基配列をDNA切断酵素(Cas9タンパク質)で切断する必要があるが、従来の技術ではDNA切断酵素の活性を制御できないため、Cas9の活性を制御できる技術開発が求められていた。
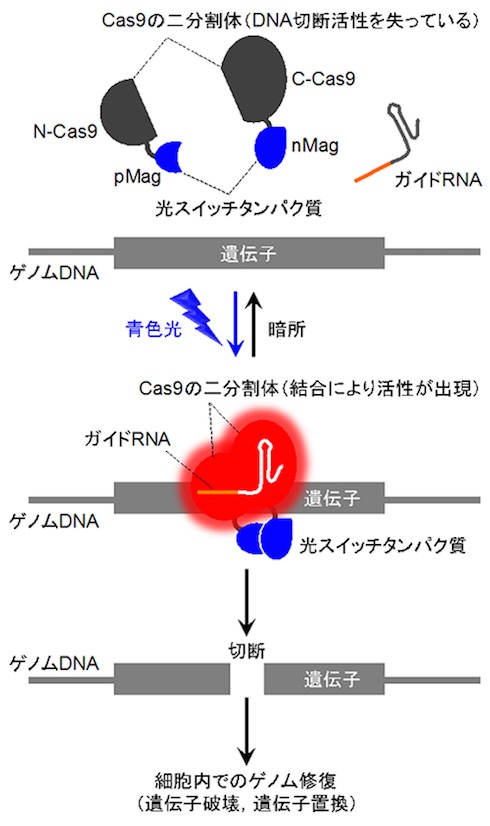
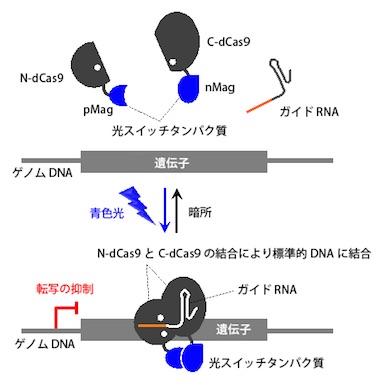
同研究グループでは、Cas9の制御を実現するため、まずCas9タンパク質を2分割してそのDNA切断活性を不活性化した。次に、2分割によって活性を失ったCas9のN末端側断片(N-Cas9)とC末端側断片(C-Cas9)に、青色の光に応答して互いに結合する小さな光スイッチタンパク質(pMag/nMag)を連結。これに青色の光を照射すると、pMag/nMagの結合に伴って、N-Cas9/C-Cas9も近づいて結合する。この結合により、N-Cas9/C-Cas9はDNA切断活性を回復し、標的の塩基配列を切断できるようになる(スイッチオン)という。光照射を止めると、pMag/nMagは結合力を失うため、N-Cas9/C-Cas9も離ればなれになり、DNA切断活性はなくなった(スイッチオフ)。
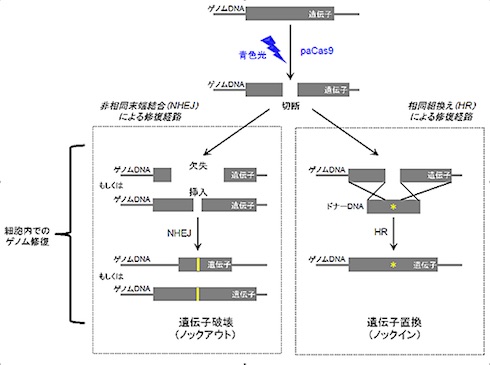
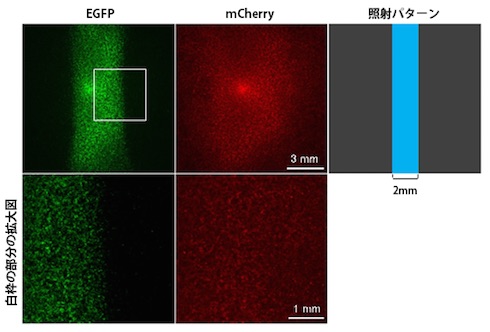
同研究では、同ツール(光活性化型Cas9(以下、paCas9))を用いて、狙ったゲノム遺伝子の塩基配列を改変し、その機能を破壊(ノックアウト)できること、また、別の塩基配列に置き換え(ノックイン)できることを示した。さらに、光照射のパターンを制御することで、ゲノム編集を空間的に制御できる(光照射した部分でだけ、ゲノム編集が行われる)ことも実証した。
CRISPR-Cas9システムを光照射のオン・オフで制御するpaCas9は、従来のゲノム編集技術の問題点を克服するものになるという。今後は、医療や創薬、育種・品種改良など、応用の可能性を大きく広げることが期待されるとしている。
Copyright © ITmedia, Inc. All Rights Reserved.
関連記事
 運転能力を低下させる白質病変、東京大学らが実車実験で確認
運転能力を低下させる白質病変、東京大学らが実車実験で確認
東京大学と高知工科大学は、医学的に症状のない軽度の大脳白質病変(以下、白質病変)と診断された高齢の運転者は、そうでない高齢の運転者に比べて、運転能力が低下していることが実車実験で確認できた、と発表した。 3Dデザイン/設計スキルを学ぶ世界イベントに東大生3人が日本代表として参加
3Dデザイン/設計スキルを学ぶ世界イベントに東大生3人が日本代表として参加
オートデスクは、製造や建築分野の3Dデザイン/設計スキルの集中トレーニングを行うワールドワイドの学生向けイベント「Autodesk Panorama」の日本代表として、東京大学の学生3人が選ばれたと発表した。 アベノミクス第3の矢を実現する10のイノベーション【前編】
アベノミクス第3の矢を実現する10のイノベーション【前編】
安倍政権が推し進める経済再生政策の「第3の矢」を実現する上で重要な役割を担っているのが、「戦略的イノベーション創造プログラム(SIP)」だ。年間予算がそれぞれ数十億円に達するSIPの10のプログラムについて、「SIPシンポジウム」の講演内容に沿って前後編に分けて紹介する。 半導体技術で“モバイル医療”の実現へ
半導体技術で“モバイル医療”の実現へ
心臓を専門とする医学研究者は、米国半導体工業会(SIA)のイベントで、心電図をリアルタイムでスマートフォンに表示できる機能などを見せ、半導体技術がもたらす医療の進歩の可能性について話した。医療/ヘルスケア分野が、半導体技術に寄せる期待は大きい。 チェス、オセロ、クイズの次は「東大」だ!! ――NII「人工頭脳プロジェクト」始動
チェス、オセロ、クイズの次は「東大」だ!! ――NII「人工頭脳プロジェクト」始動
国立情報学研究所の人工頭脳プロジェクトは「ロボットは東大に入れるか」というグランドチャレンジに向け始動。2016年までに大学入試センター試験で高得点をマーク、2021年に東京大学入試を突破を目指す。