新型コロナウイルスの糖鎖と結合し、感染を抑制する天然物を特定:医療技術ニュース
名古屋大学らは、放線菌が生産する天然物のプラディミシンAが、新型コロナウイルス表面の糖鎖と結合し、感染を抑制することを発見した。糖鎖構造はウイルス変異で変化しにくいため、さまざまな変異株に有効な抗SARS-CoV-2薬の開発が期待される。
名古屋大学は2024年7月3日、放線菌が生産する天然物のプラディミシンA(PRM-A)が、新型コロナウイルス(SARS-CoV-2)表面の糖鎖と結合し、感染を抑制することを発見したと発表した。長崎大学、広島大学、富山県立大学、大阪大学との共同研究による成果だ。
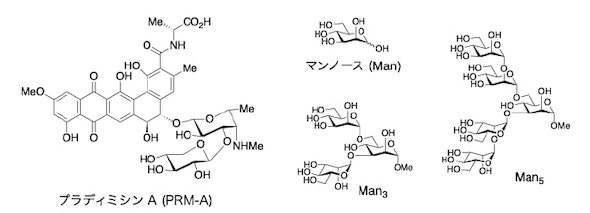
放線菌は、土壌に存在する微生物で、抗生物質を生産する能力に優れる。その放線菌が生産するPRM-Aは、糖鎖の1種であるマンノース(Man)に結合することが知られている。
そこで同研究では、SARS-CoV-2糖鎖の部分構造に対応するオリゴ糖を化学合成し、PRM-Aの結合活性を評価した。その結果、PRM-Aは、Manで構成される二分岐型オリゴ糖(Man3、Man5)に強く結合することが分かった。
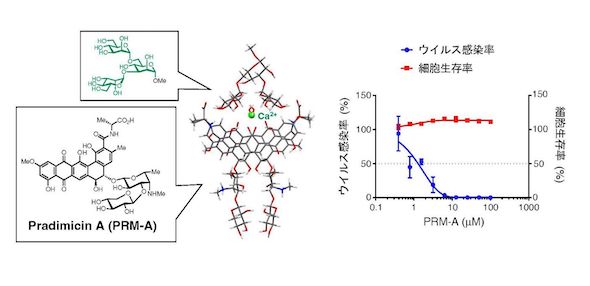
また、PRM-AとMan3が結合した複合体を解析したところ、2分子のPRM-Aがカルシウムイオンを介してまとまり、Man3の2つの分岐末端と相互作用することが示唆された。
これらの知見をベースに、ヒト気管支上皮由来のCalu-3細胞に対するSARS-CoV-2の感染阻害試験を実施。PRM-Aは、細胞毒性を示すことなく、SARS-CoV-2の感染を抑制した。この感染抑制活性は、Man3共存下では大幅に低下しており、PRM-AがSARS-CoV-2の糖鎖に結合してウイルス感染を抑制することが示された。
SARS-CoV-2糖鎖に結合して感染抑制活性を示す物質には、タンパク質のレクチンがある。一方でレクチンは、高分子タンパク質のため抗ウイルス薬として利用するには課題がある。
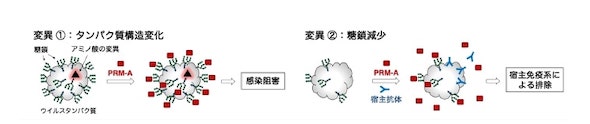
今回の研究成果で、レクチンよりも化学的に安定しており、細胞毒性などを持たない低分子化合物のPRM-Aが、糖鎖を標的とした抗SARS-CoV-2薬の候補として有望であることが示された。化学合成も可能で、また糖鎖構造はウイルス変異で変化しにくいことから、さまざまな変異株に有効な抗SARS-CoV-2薬の開発が期待される。
Copyright © ITmedia, Inc. All Rights Reserved.
関連記事
 低出力レーザーによる光濃縮で迅速かつ高感度なウイルス測定が可能に
低出力レーザーによる光濃縮で迅速かつ高感度なウイルス測定が可能に
大阪公立大学は、光濃縮技術を取り入れた「光誘導イムノアッセイ技術」を開発した。微量で低濃度なサンプルでも約5分で正確なウイルス計測が可能だ。 健康診断の心電図異常は将来の心血管疾患発症リスクと関連する
健康診断の心電図異常は将来の心血管疾患発症リスクと関連する
京都大学らは、全国健康保険協会のデータを用いて、健康診断において心電図異常が指摘されると、将来の心血管疾患の発症リスクが上昇することを明らかにした。 日本の臨床ニーズにあった椎弓形成術用のインプラントを発売
日本の臨床ニーズにあった椎弓形成術用のインプラントを発売
日本ストライカーは、頚椎症性脊髄症に対応する術式の1つである椎弓形成術に使用するインプラント「Lhotseプレート」の販売を開始した。日本人の骨格に合わせて開発され、独自の傾斜角およびサイズを展開する。 肺のCT検査画像をMRで観察できる、トレーニングシステムの提供を開始
肺のCT検査画像をMRで観察できる、トレーニングシステムの提供を開始
日本メドトロニックは、CTで撮影した肺の構造を、MRで実寸大の3D画像として観察できる医療従事者向けトレーニングシステム「MR Anatomy」の提供を開始した。 屋外活動時間を増やすことは子どもの近視発症を抑制する可能性がある
屋外活動時間を増やすことは子どもの近視発症を抑制する可能性がある
京都大学は、システマチックレビューを用いた研究により、屋外活動の時間を増やすことが子どもの近視の進行予防になるかは不明確なものの、発症予防につながる可能性が高いという研究結果を発表した。 AI医療機器やGCP査察を巡る多国間連携と働き方改革、日本のPMDAの対応は
AI医療機器やGCP査察を巡る多国間連携と働き方改革、日本のPMDAの対応は
本連載第104回で米国、カナダ、英国のAI医療機器指導原則を取り上げたが、それと並行して国境を越えた規制監督業務DXの取り組みも進んでいる。