増えない細胞だったニューロンの細胞分裂に成功、新たな脳再生医療へ:医療技術ニュース
東京医科歯科大学は、大脳皮質ニューロンの細胞分裂を妨げる仕組みを突き止め、さらにそれを解除する低分子化合物を同定し、脳梗塞モデルニューロンを細胞分裂させることに成功した。
東京医科歯科大学は2017年9月19日、大脳皮質ニューロンの細胞分裂を妨げる仕組みを突き止め、さらにそれを解除する低分子化合物を同定し、脳梗塞モデルニューロンを細胞分裂させることに成功したと発表した。同大学統合研究機構脳統合機能研究センター 准教授の味岡逸樹氏らの研究グループと愛知県心身障害者コロニー発達障害研究所との共同研究によるもので、成果は同日、英科学誌「Development」電子版に掲載された。
脳梗塞など、ニューロンが脱落する神経変性疾患では、脱落しなかったニューロンも増えず、かつ進行的に脱落するため、治療が難しい。同研究で判明した脳梗塞ニューロンの脱落を防いで細胞分裂させる方法は、新しい脳再生医療につながることが期待される。ただし現時点では、脳への悪影響やがん化の可能性もあるため、脳梗塞後に分裂したニューロンの機能を検討し、脳再生医療へ展開できるか検証を進める。
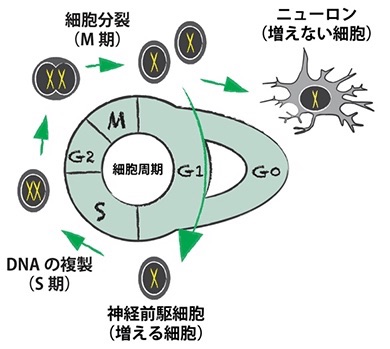
細胞分裂が起こる過程は細胞周期と呼ばれ、細胞周期には、DNA複製をするS期、細胞分裂をするM期、それらの間にG1期とG2期がある。ニューロンは、増えない細胞の代表例だ。主に胎児期に細胞分裂を繰り返す神経前駆細胞から生み出され、分化開始とほぼ同時に別の細胞周期であるG0期に入り、増えなくなると考えられている。
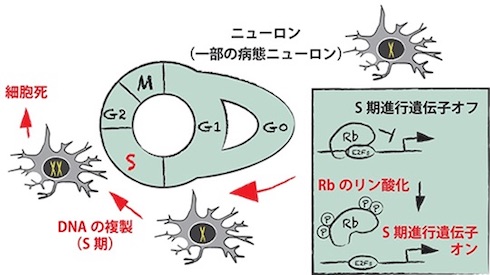
味岡准教授らのグループはこれまでに、Rbファミリータンパク質がG0期からS期へ進行しないためのブレーキとして機能し、それらを欠損させると一部のニューロンが増えることを発見していた。一方で、その他の研究から、脳梗塞やアルツハイマー病で観察されるニューロン脱落の一部は、Rbをリン酸化して細胞周期をS期へと進めてから細胞死を起こすということも知られている。
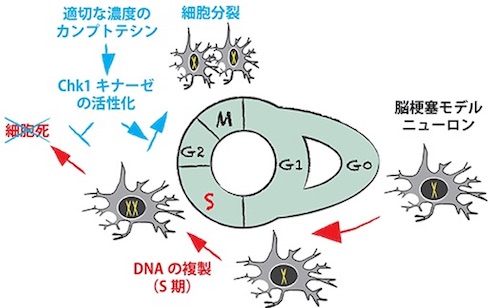
今回の研究では、まず、S期に進んでからニューロンの細胞死を誘導するRbファミリー欠損モデル(脳梗塞モデル)を確立した。そのモデルでM期へ進行する際のブレーキの仕組みを調べたところ、脳発生期のDNAメチル化酵素の作用で、Chk1キナーゼというタンパク質の機能が抑制され、ブレーキがかけられていることが分かった。
さらに、Chk1キナーゼを活性化させて、このブレーキを解除するのが低分子化合物カンプトテシンであることも見いだした。そこで脳梗塞モデルに、特定の濃度のカンプトテシンを投与したところ、細胞分裂させることに成功した。
Copyright © ITmedia, Inc. All Rights Reserved.
関連記事
 AIに最適な脳型LSI、東北大が脳機能のモジュール化で2019年度に実現へ
AIに最適な脳型LSI、東北大が脳機能のモジュール化で2019年度に実現へ
東北大学の電気通信研究所は、2014〜2019年度のプロジェクトで、AI(人工知能)に最適な脳型LSIの開発を進めている。脳機能をモジュール化して計算効率を高め、人間の脳と同等レベルの処理能力と消費電力を持つ脳型LSIの実現につなげたい考えだ。 人がモノを見たり想像したりする時の脳活動を解読、人工知能への応用も
人がモノを見たり想像したりする時の脳活動を解読、人工知能への応用も
京都大学は、ヒトの脳活動パターンを人工知能モデルの信号に変換し、どんな物体を見たり想像したりしているかを脳から解読する技術を開発した。脳からビッグデータを利用する先進的技術となり、脳型人工知能の開発が期待できる。 脳梗塞領域に血管を誘引する人工細胞足場、脳の修復や再生に寄与
脳梗塞領域に血管を誘引する人工細胞足場、脳の修復や再生に寄与
東京医科歯科大学は、脳梗塞領域に血管を誘引するスポンジ形状の人工細胞足場を開発した。一度損傷を受けると再生しないとされていた脳の修復/再生に寄与する成果で、再生医療への展開が期待される。 細胞凝集体の中に栄養や酸素を供給できる血管網、組織培養に展開可能
細胞凝集体の中に栄養や酸素を供給できる血管網、組織培養に展開可能
京都大学は、培養した組織の中に毛細血管状の管を通し、血流を模した流れによって栄養や酸素を供給できるマイクロ流体デバイスを開発した。これまで困難だった組織培養や、長期の組織観察に展開可能だという。 視細胞を制御するソフトウェアを視覚再生医療に提供
視細胞を制御するソフトウェアを視覚再生医療に提供
JIG-SAWとモビコムは、ソフトウェアで視細胞を制御する「視覚再生医療」に着手した。視覚再生用のプリズムグラスと視細胞制御ソフトウェアを提供する。