プレシジョンメディシンの鍵を握る次世代シーケンサー規制:海外医療技術トレンド(16)(1/3 ページ)
遺伝子の塩基配列を高速に読み出す次世代シーケンサー。米国では、遺伝子プロファイルを利用して各個人に合った治療法を提供する「プレシジョンメディシン」の中核技術として、臨床適用に向けたルールづくりが進んでいる。
次世代シーケンサーに係るイノベーションと規制の両立を図る米国FDA
2015年2月20日、米国食品医薬品局(FDA)は、ヒトゲノムや次世代シーケンシング(NGS)技術のための診断試験に対するFDAの規制方法について議論し、コミュニティーからフィードバックを収集することを目的として、「次世代シーケンシング診断試験に関するFDAの規制監督の最適化公開ワークショップ」を開催した(関連情報)。
次世代シーケンシングを利用した体外診断医療機器(IVD)は、本連載第2回で取り上げた「プレシジョンメディシン・イニシアチブ」(関連情報)の柱になっている。FDAは、イノベーションの創出と患者の保護の両立を図る観点から、次世代シーケンシングを規制するルールづくりの検討を行ってきた。
図1は、次世代シーケンシング試験の流れを示したものである。解析前の段階の標本からDNAを調製してライブラリーを作製した後、ソフトウェアで塩基配列解析を実施・翻訳し、ナレッジベース化するというのが、一般的な試験の流れだ。
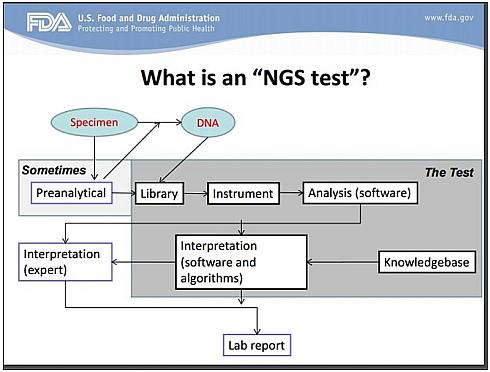
図1 次世代シーケンシング試験とは何か?(クリックで拡大)出典:FDA「Use of Standards in FDA Regulatory Oversight of Next Generation Sequencing (NGS)-Based In Vitro Diagnostics (IVDs) Used for Diagnosing Germline Diseases Draft Guidance for Stakeholders and Food and Drug Administration Staff」(2015年2月20日)
ワークショップでは、次世代シーケンシングの特徴として、以下のような点を挙げている。
- 試験で何が検知されるかをあらかじめ定義できない。
- まれな変異を検知する、前例のない能力がある
- 特定の意図された用途がない(複数の状態を同時に診断することが可能)
- 結果を医師や患者に伝達することが難しい
- 急速に進化する技術である
- 高いスループットによって理解を越えた発見が可能になる
次世代シーケンシングに基づいて分析評価する際には、適切な方法で遺伝子マーカーのサブセットを選択/検証しながら、正確性を期すことが要求される。また、ナレッジベースなど、分析評価の結果を比較/参照する手法の開発も必要だ。さらに、遺伝子性疾患、がん治療など、用途によっては、分析評価戦略の方向性を変える必要もでてくる。
Copyright © ITmedia, Inc. All Rights Reserved.