リチウムイオン電池リサイクル技術の現在地:LIBリサイクルの水熱有機酸浸出プロセス開発の取り組み(6)(3/4 ページ)
本連載では東北大学大学院 工学研究科附属 超臨界溶媒工学研究センターに属する研究グループが開発を進める「リチウムイオン電池リサイクル技術の水熱有機酸浸出プロセス」を紹介する。最終回となる第6回ではこれまでのまとめとリチウムイオン電池に関する研究論文の特徴を取り上げる。
4 超臨界CO2プロセス
超臨界CO2は31℃、7.3MPaを超えた状態のCO2を指し、無極性溶媒(例えばヘキサン)のように振る舞うものの、溶解性や拡散性は液体の無極性溶媒とは異なる性質を示す。
特に、温度を増大させ溶質の蒸気圧(もしくは昇華圧)が増大することで気体のように混じり合うようにすることができる。また、超臨界CO2の温度を40〜80℃程度とし、圧力を20MPa〜40MPaとすることで密度を液体のように高い状態にすることができ、その際に、エタノール、アセトン、アセトニトリル(CH3CN)、ジメチルスルフォキシド(DMSO)のような極性溶媒を添加することで、溶媒密度や極性を制御することができる。
また、金属イオンのように極端に水に親和的な物質は、錯体として超臨界CO2への親和性を高めるか(筆者らがJST未来創造事業で取り組んだ手法)、もしくは超臨界CO2に対して高い親和性を示す界面活性剤を添加しミセルとして、超臨界CO2に分散できるようにするといった手段が選択されることもある。
このように、温度、圧力、助溶媒(エントレーナともいう)や各種添加剤(配位子や界面活性剤)を選定し、溶解性を制御することが超臨界CO2を溶媒として用いることの意義である。さらにCO2は、大気圧、室温では気体であるため、超臨界CO2を分離溶媒として対象物質を抽出分離した場合、溶媒は散逸するため対照物質を濃縮回収することができることも、利点の1つである。
このことに加え、リチウムイオン電池リサイクルの観点における超臨界CO2(高圧状態のCO2)の特徴は、CO2が水に溶解し炭酸としてプロトン供与体となることであり、またアルカリ金属イオンであるリチウムイオンと反応し炭酸塩を形成する反応物としても作用することである。こうした超臨界CO2の特徴を生かしたリチウムイオン電池リサイクルに関連する研究が実施されている。
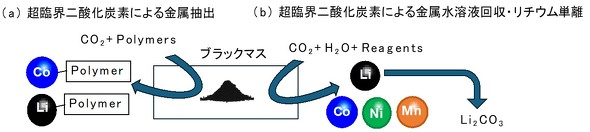
以下ではまず、廃棄リチウムイオン電池のリサイクルに対して超臨界CO2の利用を検討した報告から、正極材濃縮物(ブラックマス)を対象とした検討(図4)と、電池セルを対象とした検討(図5)に分けてそれぞれ簡潔に説明する。
4−1 ブラックマスを対象とした検討
超臨界CO2を溶媒として、リチウムイオン電池の正極材活物質に含まれる金属を抽出する研究は依然として少数である。しかし最近、配位子としてトリブチルフォスフェート(TBP)を用いた検討[参考文献47]や特殊な高分子(p[VBPDA-co-FDA]copolymers)を界面活性剤として用いCoやNiを抽出する検討[参考文献51]など、超臨界CO2中に金属イオンを抽出分離する報告がなされた(図4a)。
その一方、抽出媒体を水として超臨界状態のCO2をプロトン供給源とした研究[参考文献46]や、リチウムイオンを水熱条件の水と超臨界CO2を共存させて抽出するとともに、選択的に炭酸リチウムとして回収するプロセスの検討[参考文献48〜50]もなされている(図4b)。
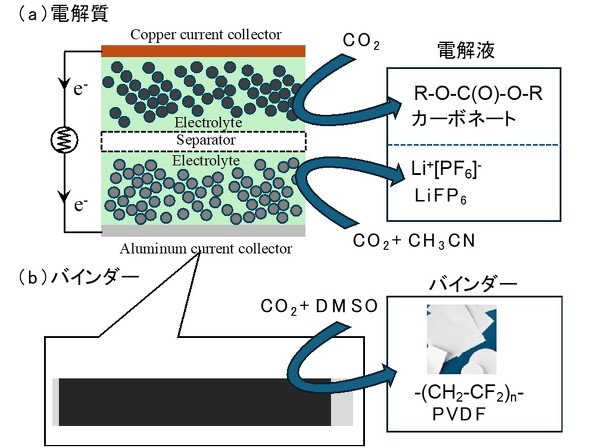
4−2 電解質抽出およびバインダー分離
リチウムイオン電池は一般的に、有機炭酸塩(ジメチルカーボネート、エチルメチルカーボネートなどの混合溶液)に、ヘキサフルオロリン酸リチウム(LiPF6)を加えた電解質が用いられている。LiPF6は水分が要因で容易に分解が促され、フッ化水素の発生とともに、非常に毒性の高いリン化合物が生成される。
この分解反応はまた、有機炭酸塩の分解/重合反応も促し、電池劣化を加速する。このことは、リサイクルプロセス構築においても十分留意を要する。すなわち、リサイクルプロセスの過程で電解質に水が混入するとLiPF6の加水分解が誘発され危険な化合物を容易に生成し、電解質の化学変性も進んでしまうため、リサイクル全体に悪影響を及ぼす。
CO2を用いるプロセスは、理想的には水の混入がなく安全に電解質を回収できるプロセスを構築し得る。実際、25℃の液体CO2(6MPa)や、40℃程度の超臨界CO2(10MPa〜23MPa)を用いることで、74〜90%程度、電解質を回収することができることが報告されている[参考文献63]。
この時、アセトニトリル(CH3CN)とプロピレンカーボネート(PC)を適宜加えることで、LiPF6を、わずかではあるが回収するできることが示された(図5a)。電解質を除去することで、正極材のみならず、負極材活物質である炭素材料も再利用できる可能性が示されている[参考文献55]。
ただし、CO2も水分を含むことがあることから、副反応を阻止するために水分量の管理が求められる。総説[参考文献64]によれば、電解質の超臨界CO2抽出には、電池劣化度合いなどにより状態が整わないこともあることから不明の点も多く、いまだに検討の余地があるとされている。
リチウムイオン電池のセルには、正極および負極それぞれの活物質を集電体に結着(けっちゃく)させるためのバインダーが用いられている。特に正極にはポリフッ化ビニリデン(PVDF)が用いられている。PVDFもまた、超臨界CO2プロセスにより電池セルから回収することができる。総説[参考文献64]によれば、超臨界CO2にジメチルスルフォキシド(DMSO)を加えた系で、70℃、8MPa、13分間処理することでPVDFが99%回収できると報告されている(図5b)。
Copyright © ITmedia, Inc. All Rights Reserved.