ヘルペスが繰り返し発症する理由は、「宿主の免疫から逃げる分子メカニズム」:医療技術ニュース
東京大学は、単純ヘルペスウイルスの新しい免疫回避機構を発見し、それをつかさどるウイルスタンパク質として「VP22」を同定した。解明された分子メカニズムを標的としたHSV感染症の新しい治療法の開発につながる。
東京大学は2018年2月15日、同大学医科学研究所 教授の川口寧氏らの研究グループが、単純ヘルペスウイルス(HSV)の新しい免疫回避機構を発見し、それをつかさどるウイルスタンパク質として「VP22」を同定したと発表した。
HSVは一度感染すると、宿主の免疫応答によって体内から排除されることなく、ヒトの体内に終生潜伏する。そのため、HSV感染症は多くの病態において潜伏と再発を繰り返す。このことから、HSVにはヒトの多様な免疫応答から逃れる高度な機構があると考えられている。
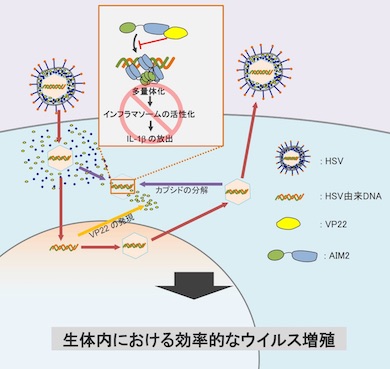
そして、AIM2インフラマソームに対するHSV阻害因子の存在が長い間示唆されてきた。AIM2インフラマソームは、DNAセンサータンパク質であるAIM2がDNAを認識し、多量体化することが引き金となって形成される巨大タンパク質複合体だ。さまざまな病原体由来のDNAによって活性化され、生体内での病原体感染の阻害に関わるインターロイキン1β(IL-1β)やIL-18を細胞外へ放出する。これは重要な自然免疫応答だ。しかし、HSVはDNAを遺伝子として持つが、AIM2インフラマソームが活性化されないと分かっている。他の病原体を含め、AIM2インフラマソーム阻害因子はまだ同定されていなかった。
同研究では、まず、細胞にAIM2インフラマソームの構成因子、未成熟型IL-1β、72種類のHSVタンパク質をそれぞれ発現させ、培養上清に放出されたIL-1βを測定した。その結果、AIM2インフラマソームを阻害するHSV因子としてVP22を同定した。VP22はAIM2と結合し、その多量体化を抑制することで、AIM2インフラマソームの活性化を阻害していることも分かった。
次に、AIM2欠損細胞と野生型細胞に、VP22欠損ウイルスと野生型ウイルスを感染させた。VP22欠損ウイルスの場合は、DNAを遺伝子として持つ他の病原体と同様に、AIM2があればインフラマソームの活性化が起こった。野生型ウイルスの感染では、どちらの細胞でもインフラマソームの活性化は認められなかった。
最後に、AIM2欠損マウスと野生型マウスの脳内に、VP22欠損ウイルスと野生型ウイルスを接種し、ウイルス増殖を比較した。VP22欠損ウイルスの場合、AIM2欠損マウスでは脳内ウイルス力価が顕著に上昇していた。一方、野生型ウイルスの感染では、ウイルス力価に有意な差は認められなかった。以上の結果は、VP22によるAIM2インフラマソームの阻害が、生体内におけるウイルス増殖に重要であることを示す。
これによりHSVが宿主の免疫応答から逃れる新しい分子メカニズムが解明され、ウイルス病態が何度も再発する仕組みの一端が明らかになった。また、この成果は、解明された分子メカニズムを標的としたHSV感染症の新しい治療法の開発につながることが期待される。
Copyright © ITmedia, Inc. All Rights Reserved.
関連記事
 マイタケ由来タンパク質がインフルエンザウイルスの増殖を抑制
マイタケ由来タンパク質がインフルエンザウイルスの増殖を抑制
理化学研究所は、食用キノコのマイタケから、脂質ラフトと呼ばれる動物細胞膜上の脂質構造に結合するタンパク質を発見。その存在下ではインフルエンザウイルスの増殖が抑えられることを明らかにした。 インフルエンザウイルスが子孫に遺伝情報を伝える仕組みを解明
インフルエンザウイルスが子孫に遺伝情報を伝える仕組みを解明
東京大学は、インフルエンザウイルスが子孫ウイルスに遺伝情報を伝える仕組みを明らかにした。ウイルス内の8本のRNAを「1+7」に集合させる過程が重要であることが分かった。 ウイルス粒子を光と動きで検出するバイオセンサーを開発
ウイルス粒子を光と動きで検出するバイオセンサーを開発
産業技術総合研究所は、「外力支援型近接場照明バイオセンサー」を開発した。夾雑物を含む試料中のごく少量のバイオ物質を、夾雑物を除去しなくても高感度に検出でき、ウイルス感染予防への貢献が期待される。 薬剤耐性B型肝炎にも作用する治療薬の開発へ、エイズウイルスが貢献
薬剤耐性B型肝炎にも作用する治療薬の開発へ、エイズウイルスが貢献
産業技術総合研究所は、ヒト免疫不全ウイルス(HIV)を用いて、現在B型肝炎治療に広く用いられている核酸アナログ製剤「エンテカビル」が作用する仕組みと、薬剤耐性が生じる仕組みを明らかにした。 エアコンがインフルエンザを検知!? 産総研が小型高感度のウイルスセンサーを開発
エアコンがインフルエンザを検知!? 産総研が小型高感度のウイルスセンサーを開発
産業技術総合研究所は、インフルエンザウイルスを検出できる小型高感度センサーの開発に成功したと発表した。従来1日半以上を要したウイルス検出時間を数十秒レベルに短縮でき、将来は空気中のウイルス検知も可能になるという。